Universidade de Trás-os-Montes e Alto Douro
Produtos da Reação de Maillard em produtos de panificação: efeito do processamento e composição
Dissertação de Mestrado
Mestrado em Segurança Alimentar
Ângela Liquito Ferreira de Sousa
Orientador: Professora Doutora Maria Cristina Guiomar Antunes
ii
Universidade de Trás-os-Montes e Alto Douro
Produtos da Reação de Maillard em produtos de panificação: efeito do processamento e composição
Dissertação de Mestrado em Segurança Alimentar
Ângela Liquito Ferreira de Sousa
O Orientador
_________________________________ (Prof.ª Doutora Maria Cristina Guiomar Antunes)
Departamento de Química/UTAD
O Arguente
_________________________ (Prof.ª Doutora Alice Vilela)
Departamento de Enologia/UTAD
A Direção de Mestrado
_______________________ __________________________ (Prof.º Doutor Luís Patarata) (Prof.º Doutor José António Silva)
Departamento de Ciências Agrárias/UTAD
iii
“As doutrinas apresentadas no presente trabalho são da exclusiva responsabilidade do autor.”
iv
Agradecimentos
Aos meus pais pela oportunidade de continuar mais um nível académico, onde aumentei o meu conhecimento todos os dias que passei na UTAD e na cidade de Vila Real. Não esquecendo o apoio e incentivo para ir mais além.
Aos meus avós pelo apoio, suporte e orgulho em mim.
Á Professora Doutora Cristina Guimoar Antunes por ter aceite o convite de trabalhar comigo, pela dedicação, carinho, ajuda e paciência.
Ao Professor Doutor Carlos Ribeiro que esteve presente desde o 1º ano de licenciatura até ao fim do Mestrado, que nos mostra que quando nos esforçamos, somos capazes.
Ao técnico de laboratório, Sr. Carlos Matos, pela companhia em laboratório, pelo tempo disponibilizado, pela ajuda preciosa e dedicação para sucesso do meu trabalho.
Ao Professor Doutor Luís Ferreira e à Ana Abraão por cederem o laboratório de nutrição animal.
À Professora Doutora Alice Vilela pela amizade e prontidão em reunir o painel de provadores para complementar o meu trabalho prático.
Ao painel de provadores (Alice Vilela, António Inês, António Lage, Miguel Bacelar, Carla Amaral, Berta Gonçalves, Eunice Bacelar, Edna Cabecinha, Paula Ribeiro, Rosário Anjos, Teresa Pinto, José Albino Sá, Andreia Matos, Ana Gouveia, Rui Costa) que incansavelmente compareceu às provas, sempre com boa disposição.
Aos meus amigos pelos momentos universitários e que sempre me apoiaram e incentivaram a fazer o meu melhor e que nesta última fase reforçaram a preocupação e carinho, quero salientar alguns nomes Ângela Rocha, Joana Vilela, Liliana Silva, Soraia Pinto, Paula Sampaio.
Por fim, quero agradecer à instituição Universidade de Trás-os-Montes e Alto Douro e à cidade de Vila Real por me terem acolhido tão bem e pelas experiências da escola da vida.
v
Índice de Figuras ix
Índice de Tabelas xi
Lista de Abreviaturas xii
Resumo xiii Abstrat xv Capítulo I ... 1 Revisão Bibliográfica ... 1 1. Enquadramento temático 2 1.2 Alimentação e Saúde 2 1.3 Alimentos funcionais 3 1.4 O Pão 6 1.4.1 Tipos de Pão 7
1.5 Caraterísticas e funções dos constituintes do pão 9
1.5.1 Farinha 9
1.5.2 Gelatinização do amido 12
1.5.3 Gelificação e retrogradação do amido 13
1.6 Água 14 1.7 Sal 15 1.8 Levedura 15 1.9 Farinhas em estudo 16 1.9.1 Chia 17 1.9.2 Maçã 18 1.9.3 Quinoa 19 1.9.4 Linhaça 21 1.10 Processamento térmico 23 1.10.1 Reação de caramelização 24 1.10.2 Reação de Maillard 25
1.10.3 Marcadores da reação de Maillard 28
1.10.3.1 Cor 29
1.10.3.2 5-Hidroximetilfurfural e furfural 29
1.10.3.3 Compostos intermediários fluorescentes 30
1.11 Implicações dos produtos da reação de Maillard na saúde 30
1.12 Validação do Método 33
1.12.1 Curva de calibração 33
vi 1.12.4 Limite de deteção 34 1.12.5 Limite de quantificação 34 1.12.6 Exatidão 35 1.12.7 Repetibilidade 35 1.12.8 Precisão 35 1.12.9 Precisão Intermédia 36
1.13 Qualidade sensorial no Pão 36
Capítulo II ... 37 Objetivos ... 37 Objetivos 38 Capítulo III ... 39 Material e Métodos ... 39 3.1 Reagentes e padrões 40 3.2 Amostras 40
3.2.1 Preparação dos pães 40
3.2.2 Armazenamento das amostras 42
3.3 Preparação das soluções padrão 42
3.3.1 Preparação da solução padrão de HMF 42
3.3.2 Preparação da solução padrão de Furfural 42
3.3.3 Preparação da solução padrão de catequina 42
3.3.4 Preparação da solução padrão de ácido gálico 43
3.3.5 Preparação da solução padrão de Trolox 43
3.3.6 Preparação da solução padrão de DPPH 43
3.3.7 Preparação da solução padrão de ABTS 43
3.3.8 Preparação da solução de EDTA 43
3.3.9 Preparação da solução DAN 44
3.3.10 Preparação das soluções padrão de metais 44
3.4 Determinação do teor de humidade 44
3.5 Medição do pH 44
3.6 Medição da Atividade de Água (Aw) 45
3.7 Compostos bioativos 45
3.7.1 Extração dos compostos bioativos 45
3.7.2 Determinação dos compostos fenólicos 46
3.7.3 Determinação do teor de flavonóides totais 48
3.8 Marcadores da Reação de Maillard 49
3.8.1 Extração dos marcadores da RM 49
vii
3.8.4 Determinação de compostos fluorescentes 51
3.8.5 Medição da cor 52
3.9 Determinação da capacidade antioxidante 53
3.9.1 Método DPPH 53
3.9.2 Método ABTS 55
3.10 Determinação de metais 55
3.10.1 Determinação de metais por Espectroscopia Atómica 55
3.10.2 Preparação da amostra 56
3.10.3 Análise das amostras e condições operatórias 58
3.11 Determinação de selénio 59
3.11.1 Determinação de selénio por Espectroscopia de Fluorescência 59
3.11.2 Preparação da amostra 59
3.11.3 Análise das amostras e condições operatórias 60
3.12 Determinação das características químicas das amostras 60
3.12.1 Teor de matéria seca e teor de humidade 60
3.12.2 Teor em Cinza 61
3.12.3 Teor em Proteína 61
3.12.4 Determinação da fibra total 63
3.18 Determinação da Gordura bruta 64
3.21 Densidade 65
3.22 Análise Sensorial 66
3.22.1 Painel de provadores 66
3.22.2 Avaliação sensorial das amostras de pão 66
3.22.3 Análise estatística 66
3.23 Questionário on-line 67
Capítulo IV ... 68 Resultados e Discussão ... 68
4.1. Marcadores da Reação de Maillard 69
4.1.1. Teor de humidade 69
4.1.2. Atividade da água (aw) 73
4.1.3. Medição do pH 77
4.1.4. Compostos fluorescentes 78
4.1.5. Medição das absorvâncias a 280 e 420 nm 82
4.1.5. Medição da cor 85
4.1.6. Teor de HMF 93
4.2. Compostos bioativos 98
viii 4.2.3. Atividade antioxidante 101 4.3. Determinação de metais 104 4.4. Propriedades químicas 107 4.5 Análise sensorial 110 4.16 Questionário on-line 122 Capítulo V ... 124 Conclusão ... 124 Capítulo VI ... 127 Referências Bibliográficas ... 127 Anexos ... 137
ix
Figura 1 - Composição de um grão de cereal 10
Figura 1.2 - Diagrama representativo da formação da rede de glúten a partir da glutenina e gliadina (adaptado de Bobbio e Bobbio, 2001) 11
Figura 1.3 - Estruturas químicas de a) amilose e da b) amilopectina 12
Figura 1.4 - Planta (a) e sementes (b) de chia (Tosco, 2004) 17
Figura 1.5 - Maçã golden (a) e farinha de maçã (b) 19
Figura 1.6 - Planta (a) e grão (b) da quinoa (FAO, 2013) 20
Figura 1.7 - Planta com flor de coloração azul clara (a) e sementes (b) de linhaça 23
Figura 1.8 - Reação de caramelização 25
Figura 1.9 - Esquema da Reação de Maillard 26
Figura 1.10 - Estrutura química do HMF 29
Figura 1.11 - Estrutura química do furfural 30
Figura 1.12 - Formação de AGE's 32
Figura 3.1 - Sementes (a) e farinha (b) de quinoa 41
Figura 3.2 - Massa de linhaça (a) e chia (b) sem levedar 41
Figura 3.3 - Massa de linhaça (a) e chia (b) ao fim de 1h de levedação 41
Figura 3.4 - Aspeto do pão feito em laboratório e cozido em forno elétrico 42
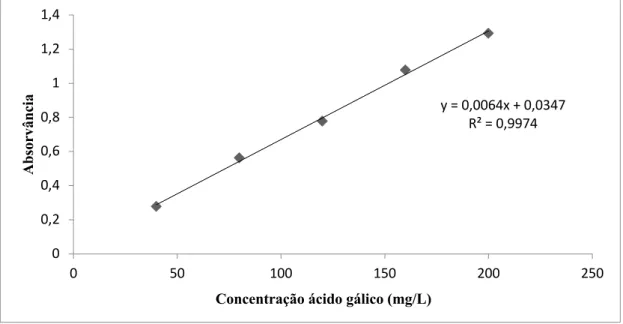
Figura 3.5 - Reta de calibração referente à gama alta de trabalho utilizada para determinar os compostos fenólicos 47
Figura 3.6 - Reta de calibração referente à gama baixa de trabalho utilizada para determinar os compostos fenólicos 47
Figura 3.7 - Reta de calibração utilizada para determinar o teor de flavonóides totais 48
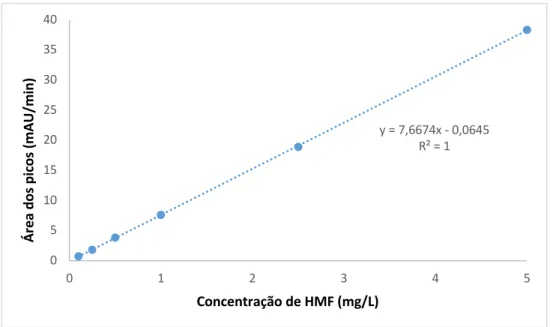
Figura 3.8 - Reta de calibração utilizada para determinar o teor de HMF nas amostras 50
Figura 3.9 - Reta de calibração utilizada para determinar o teor de furfural nas amostras 50
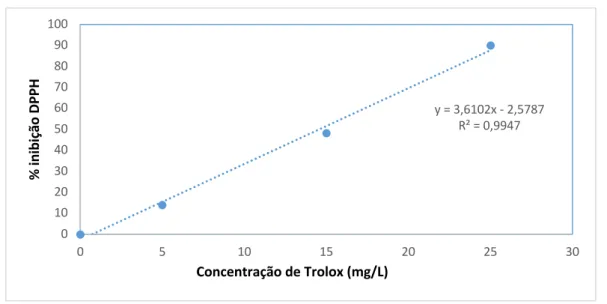
Figura 3.10 - Reta de calibração utilizada para determinar o teor de compostos fluoresecentes 52 Figura 3.11 - Colorímetro utilizado na mediação da cor das amostras de pão e das massas cruas Figura 3.12 - Reta de calibração para determinar o teor de antioxidantes através do método DPPH 54
Figura 3.13 - Reta de calibração para determinar o teor de antioxidantes através do método de ABTS 53
Figura 3.14 - Etapa da preparação amostra 60
Figura 3.15 - (a) Couvete do flourímetro para onde se retira 2 mL do dereivatizado de cada amostra; (b) flourímetro utilizado na quantificação do selénio das amostras 60
SYSTEM 1026 Destiling Unit 62
Figura 3.17 - Tecator a 110 ºC e copos de aluminio com a respetiva gordura 65
Figura 4.1 - Comparação do teor de humidade entre as várias padarias 71
Figura 4.2 - Resultados do teor de humidade em amostra de pão 71
Figura 4.3 – Resultados do teor de humidade das amostras de laboratório 73
Figura 4.4 - Resultados dos compostos fluorescentes presentes nos pães confecionados pelas padarias, expressos em eq. de sulfato de quinino 80
Figura 4.5 – Resultados dos compostos fluorescentes da Padaria 8E, expressos em eq. de sulfato de quinino 80 Figura 4.6 - Resultados dos compostos fluorescentes do pão de laboratório 82
Figura 4.7 – Resultados da leitura das absorvância a 420 nm. 85 Figura 4.8 - Resultados da leitura das absorvâncias a 420 nm. 85 Figura 4.9 – Variação global da cor dos pães preparados no laboratório 93
Figura 4.10 – Concentração de HMF (mg de HMF/100 g) de pão 94
Figura 4.11 – Concentração de HMF (mg de HMF/100 g) de pão 96
Figura 4.12 – Resultados da concentração de compostos fenólicos 99
Figura 4.13 - Resultados do teor de flavonóides presentes no pão 101
x Figura 4.16 - Dendograma (análise de clusters, pela distância Euclidiana média, método UPGMA - unweightes pair-group average) dos diferentes pães de quinoa, linhação, chia e maçã 113 Figura 4.17 - Projeção da cov-ACP dos atributos sensoriais das amostras de pães de diferentes farinhas (linhaçã, chia, quinoa e maçã), avaliadas sensorialmente (A); Projeção da cov-ACP das
amostras de diferentes farinhas (linhaça, chia, quinoa e maçã) (B) 114
Figura 4.18 - Médias das respostas de intenção de compra, por provador para o pão de chia116 Figura 4.19 - Médias das respostas de intenção de compra, por provador para o pão de quinoa
116 Figura 4.20 - Médias das respostas de intenção de compra, por provador para o pão de linhaça
117 Figura 4.21 - Médias das respostas de intenção de compra, por provador para o pão de maçã
xi Tabela 1.1 - Componentes químicos envolvidos em alguns mecanismos de ações benéficos
causados pela ingestão de alimentos funcionais 4
Tabela 1.2 - Intervalo de variação da concentração dos principais componentes do trigo
(Pallarés et al., 2007) 11
Tabela 3.1 - Pârametros de validação dos métodos 51
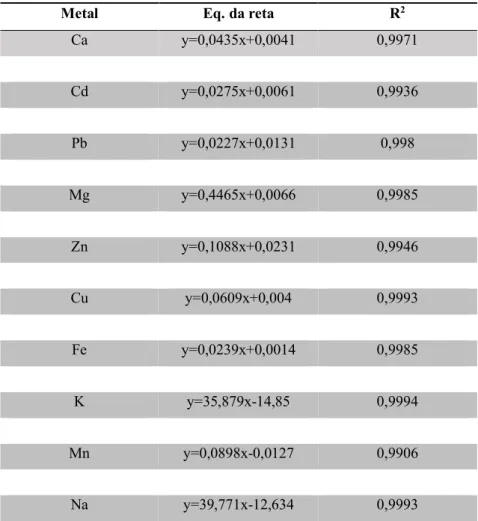
Tabela 3.2 – Gama de concentração, comprimentos de onda e tipo de atomizador para a quantificação dos metais 56 Tabela 3.3 - Equações das retas de calibração para quantificação dos metais 58
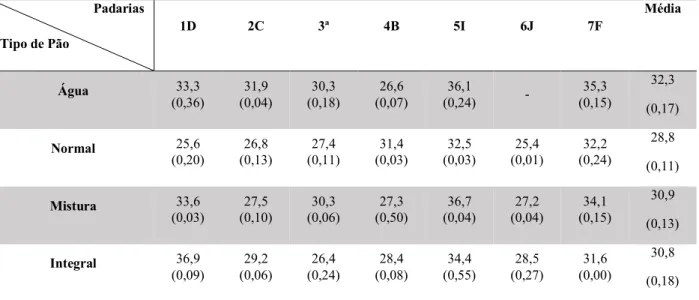
Tabela 4.1 - Média do teor de humidade (%) das amostras de pão comercializado am padarias 70 Tabela 4.2 - Resultados do teor de humidade das amostras de pão preparadas no laboratório 72 Tabela 4.3 - Medição da aw da côdea das amostras de pão das padarias 74
tabela 4.4 - Medição da aw do miolo do pão das padarias 75
Tabela 4.5 - Medição da aw dos pães das padarias 75
Tabela 4.6 - Medição da aw de pão cozido em forno elétrico e em lenha 76
Tabela 4.7 - Medição da aw de amostras de laboratório 76
Tabela 4.8 - Variação do pH durante o processo de fabrico do pão 77
Tabela 4.9 - Compostos fluorescentes livres nos pães adquiridos nas padarias 79
Tabela 4.10 - Resultados dos compostos fluorescentes do pão produzido em laboratório 81
Tabela 4.11 – Resultados das leituras das absorvâncias (A) lidos a 280 nm e 420 nm 83
Tabela 4.12 – Resultados das absorvâncias a 420 nm do pão das padarias 84
Tabela 4.13 – Resultados da cor (L) da côdea do pão das padarias 86
Tabela 4.14 - Resultados da cor (L) do miolo do pão das padarias 87
Tabela 4.15 - Resultaas da cor (a) da côdea do pão das padarias 88
Tabela 4.16 - Resultados da cor (a) do miolop do pão das padarias 88
Tabela 4.17 - Resultados da cor (b) da côdea do pão das padarias 89
Tabela 4.18 - Resultados da cor (b) do miolo do pão das padarias 90
Tabela 4.19 - Resultadosda cor da côdea e do miolo do pão 90
Tabela 4.20 - Resultados da cor da côdea e do miolo do pão 91
Tabela 4.21 - Resultados do teor de HMF nos pães das padarias 93
Tabela 4.22 - Resultados do teor de furfural nos pães das padarias 95
Tabela 4.23 - Resultados dos teores de HMF e furfural nos pães preparados no laboratório 97
Tabela 4.24 - Resultados dos teores de compostos fenólicos das amostras (em mg/g) 98
Tabela 4.25 - Resultados do teor de flavonóides 100
Tabela 4.26 - Resultados do teor de antioxidantes 102
Tabela 4.27 - Resultados dos teores de metais do pão das padarias 104
Tabela 4.28 - Resultados dos teores de metais em farinhas 106
Tabela 4.29 - Resultados dos teores de metais do pão 106
Tabela 4.30 - Resultados da composição das farinhas e dos pães 108
Tabela 4.31 - Média e desvio padrão da pontuação de cada atributo após análise sensorial das quatro amostras de pão. Amostras de pão com a mesma letra não são significativamente diferentes em relação ao atributo avaliado (teste de Duncan para P£0,05). 112 Tabela 4.32 – Fatores das coordenadas das variáveis com base nas correlações 115
xii
°C - Grau Celcius µL - Microlitro a.C. – antes de Cristo
ACIP - Associação do Comércio e da Indústria de Panificação ANOVA – Analysis Of Variance
aw – Atividade da Água
CO2 - dióxido de carbono
ESQ – equivalentes de sulfato de quinino
FAO - Organização das Nações Unidas para a Alimentação e a Agricultura g - Grama
HMF - 5-hidroximetilfurfural
HPLC – Cromatografia Líquida de Alta Eficiência Kcal - Quilocalorias Kg - Kilograma L- Litro LD – Limite de Deteção LQ – Limite de Quantificação mg- Miligrama min. - minuto mL- Mililitro MO - Matéria Orgânica MS - Matéria Seca nm- Nanómetro
PRM - produtos da reação de Maillard R2 – Coeficiente de correlação
RM – Reação de Maillard seg. – segundo
xiii Durante o cozimento de pão, ocorrem reações complexas responsáveis pelas alterações observadas na massa. Entre estas reações destaca-se a caramelização e a reação de Maillard (R. M.).
A ocorrência da RM nos alimentos assim como a sua extensão depende de alguns parâmetros, tais como, composição do alimento e tipo de processamento térmico. O trabalho realizado pretendeu determinar o teor de hidroximetilfurfural (HMF), o teor em flavonóides, compostos fluorescentes e fenólicos, pH, densidade, atividade de água e antioxidante e metais em quatro variedades de pão, entre as quais, pão normal/bijou, pão de água, pão de mistura e pão integral da cidade de Vila Real e de pão desenvolvido em laboratório, com farinhas de linhaça, maçã, quinoa e chia, de forma a estudar as suas caraterísticas.
Conclui-se que o pão de água tem o maior teor de humidade, no entanto quando cozido em forno de lenha reduz significativamente o valor.
Em relação ao pH, a massa crua da maçã foi exceção, pois aumentou relativamente à farinha, devido ao seu pH ácido e de já se encontrar misturada com a farinha de trigo.
Os valores obtidos nos compostos fenólicos variaram entre 0,58 (trigo) e 1,39 (maçã) de EAG mg/g na farinha, baixando significativamente nas massas cruas para 0,13 e 0,25, no trigo e maçã respetivamente.
O pão de mistura obteve na média de 7 padarias 0,07 mg/g de sulfato de quinino. Seguiu-se o pão de Maçã com 0,06 mg/g em teor de compostos fluorescentes.
Os teores em flavonóides na farinha variam entre 7,67 e 123,5 EQC (µg/g), pertencendo ao trigo e à maçã, respetivamente. Durante o cozimento do pão, os valores diminuíram, oscilando entre 6,40 e 17,4 EQC (µg/g), correspondendo à linhaça e à chia. Na formação de compostos acastanhados (melanoidinas), as absorvâvias a 280 nm variam nas farinhas entre 0,38 e 0,78, as massas cruas entre 0,66 e 0,85 e os pães entre 0,46 e 0,77, ou seja, é durante a levedação que se encontra menos variação entre os tipos de amostras, no entanto, é nas massar cruas (maçã) que observamos o maior teor em melanoidinas.
Na absorvância a 420 nm, o pão integral e de mistura apresentam um valor médio de 0,043 de melanoidinas. Por sua vez, o pão de linhaça, quinoa e chia obtiveram uma média de 0,007, um valor bastante inferior.
xiv trolox, tendo obtido valores compreendidos entre 0,26 e 0,27 mM/g nas farinhas e 0,14 e 0,21 mM/g equivalentes de trolox nos pães.
Em termos de propriedades químicas, os valores dos 5 tipos de pão rondam em média de 97,5 mg/g em matéria orgânica, enquanto na proteína bruta os valores obtidos são mais consistente no pão que na farinha, e variam entre 12,9-14,9 e 3,47-24,3 respetivamente.
Os teores em fibra total nas farinhas variaram entre 4,42 (trigo) e 16,3 (maçã). Os teores dos metais estudados mostram uma ordem de grandeza em ferro, zinco e cobre nas farinhas de linhaça, quinoa e chia.
No estudo, os teores de chumbo e cádmio nas farinhas são inferiores ao limites máximos pela Comissão Europeia. O selénio foi o metal menos presente nas amostras.
Através da análise sensorial destaca-se o pão de chia pelos descritores: cor do miolo, intensidade de aroma, flavour intenso e textura compacta, enquanto o pão de maçã pelo seu sabor adocicado, maciez e humidade.
Palavras-Chave: pão, farinhas, linhaça, maçã, chia, quinoa, reação de Maillard,
xv During bread baking, complex reactions occur that are responsible for the changes observed in the dough. Among these reactions, the caramelization and the Maillard reaction (R.M.) are noteworthy.
The occurrence of MRI in food as well as its extent depends on some parameters, such as food composition and type of thermal processing.
The objective of this work was to determine the content of hydroxymethylfurfural (HMF), flavonoids, fluorescents and phenolics, pH, density, water and antioxidant activity and metals in four varieties of bread, including plain bread / bijou bread of water, bread of mixture and integral bread of the city of Vila Real and of bread developed in laboratory, with flours of flax, apple, quinoa and chia, in order to study its characteristics.
It is concluded that the bread of water has the highest moisture content, however when cooked in a wood oven significantly reduces the value.
In relation to pH, the raw mass of the apple was an exception because it increased relative to the flour due to its acidic pH and already mixed with the wheat flour.
The values obtained in the phenolic compounds varied between 0.58 (wheat) and 1.39 (apple) of EAG mg / g in the flour, dropping significantly in the raw masses to 0.13 and 0.25, in the wheat and apple respectively.
The bread mix obtained on average 7 bakeries 0.07 mg / g of quinine sulfate. Apple bread was followed at 0.06 mg / g by fluorescent content.
The flavonoid contents in the flour vary between 7.67 and 123.5 EQC (µg / g), belonging to wheat and apple, respectively. During baking the values decreased, ranging from 6.40 to 17.4 EQC (µg / g), corresponding to flaxseed and chia.
In the formation of brownish compounds (melanoidines), the absorbances at 280 nm vary in the flours between 0.38 and 0.78, the raw masses between 0.66 and 0.85 and the loaves between 0.46 and 0.77, or it is during the yeast that there is less variation among the sample types, however, it is in the raw masses (apple) that we observe the highest melanoidin content.
At the absorbance at 420 nm, whole-grain and blended bread have an average value of 0.043 of melanoidines. In turn, the linseed, quinoa and chia bread obtained an average of 0.007, a much lower value.
xvi having obtained values between 0.26 and 0.27 mM / g in the flour and 0.14 and 0.21 mM / g equivalent of trolox in the loaves.
In terms of chemical properties, the values of the 5 types of bread average around 97.5 mg / g in organic matter, while in the crude protein the values obtained are more consistent in the bread than in the flour, and they vary between 12,9- 14.9 and 3.47-24.3 respectively.
Total fiber contents in the flours varied between 4.42 (wheat) and 16.3 (apple). The contents of the studied metals show an order of magnitude in iron, zinc and copper in the flours of flax, quinoa and chia.
In the study, the levels of lead and cadmium in meal are below the ceilings by the European Commission. Selenium was the least present metal in the samples.
Through the sensorial analysis the chia bread is highlighted by the descriptors: crumb color, intensity of aroma, intense flavor and compact texture, while apple bread for its sweet taste, softness and moisture.
Keywords: bread, flour, linseed, apple, chia, quinoa, Maillard reaction,
CAPÍTULO I
REVISÃO BIBLIOGRÁFICA
2 O pão é um alimento saudável, com alto teor de fibra que ingerido em quantidades adequadas apresenta benefícios para a saúde. Pertence ao grupo dos cereais, é rico em minerais, vitaminas e hidratos de carbono de absorção lenta e encontra-se na base da pirâmide da alimentação. O pão é uma fonte generosa de fibra e hidratos de carbono dois nutrientes essenciais ao nosso bem-estar. É um alimento que contém pouca gordura e se for de origem integral, possui uma dose extra de fibras, minerais e vitaminas, especialmente em vitaminas B1, essencial ao bom funcionamento do nosso sistema nervoso, do coração e auxiliando no metabolismo da glicose.
A variedade de pães atualmente disponíveis, quer em forma quer em composição, é cada vez maior e renovou a imagem tradicional do pão tornando-o um produto apreciado por um maior número de consumidores.
O consumidor de hoje está mais informado e exigente com a alimentação e, por isso, mais atento com as características dos alimentos e do seu contributo para o seu bem-estar e melhoria da saúde. Atualmente é aceite que a dieta alimentar tem uma influência decisiva na saúde do indivíduo e da população, tendo um papel crucial na manutenção e prevenção de diversas doenças, sendo este o novo conceito de alimentação saudável. Com efeito, é reconhecido que existem na dieta componentes alimentares, para além dos tradicionais, que tendem a melhorar o estado de saúde e a reduzir o risco de doença. Os alimentos que contêm estes componentes alimentares são designados por “alimentos funcionais”.
A variedade cada vez maior de pães atualmente disponíveis, quer em aspeto quer em composição, renovou a imagem tradicional do pão tornando-o um produto mais apreciado por um maior número de consumidores. Entre os vários tipos de pão destacam-se o pão de trigo, o pão de centeio, o pão integral e o pão de milho. Dada a importância do pão na dieta, a utilização de ingredientes funcionais na sua preparação tem uma elevada importância para oferecer aos consumidores alimentos diversificados com melhor qualidade nutricional e promover uma alimentação saudável.
1.2 Alimentação e Saúde
Segundos dados publicados em 2014 pela Organização Mundial de Saúde (OMS) as doenças crónicas não transmissíveis contribuíram para quase 60% das mortes em todo o mundo e é esperado que em 2020 representem cerca de 75% (OMS, 2015). Em Portugal, de acordo com o relatório da OMS, mais de 80% das mortes em Portugal resultam de doenças crónicas não transmissíveis, com as doenças cardiovasculares a
3 surgirem como as principais responsáveis. Tendo em conta estes valores a prevenção destas doenças constituí atualmente um dos maiores desafios para a saúde pública.
Os principais fatores de risco, das doenças crónicas não transmissíveis, incluem hipertensão, consumo de tabaco e bebidas alcoólicas, deficiência em ferro, colesterol sanguíneo elevado, consumo inadequado de frutos e hortícolas, inatividade física e excesso ponderal. Hábitos alimentares pouco saudáveis e inatividade física estão entre as principais causas para o aumento dos fatores de risco referidos e, consequentemente, para o aparecimento de doenças crónicas como a obesidade, doenças cardiovasculares, diabetes mellitus tipo 2 e certos tipos de cancro, que contribuem de forma significativa para as despesas globais com a saúde e para a taxa de mortalidade. Do exposto, conclui-se que a dieta constitui um fator de risco, talvez mesmo um dos mais importantes, conclui-sendo importante a consciencialização da população para a influência da alimentação e da atividade física na saúde e na redução dos fatores de risco para as doenças crónicas.
Assim, promover a saúde e bem-estar e reduzir os riscos de doenças crónicas é atualmente o conceito de alimentação saudável. Os resultados de algumas investigações científicas têm corroborado a ideia de que alguns alimentos, ou componentes alimentares tendem a melhorar o estado de saúde, o bem-estar e a reduzir o risco de doença, para além de fornecer os nutrientes essenciais (Ortega, 2006; Marques et al., 2012). É neste contexto que é introduzido o conceito de Alimento Funcional. Este conceito surgiu no Japão na década de 80, através de um programa do governo para o desenvolvimento de alimentos específicos para promover a saúde ou reduzir o risco de doença de forma a melhorar a qualidade de vida da população que envelhecia e que apresentava uma elevada esperança média de vida.
1.3 Alimentos funcionais
Embora existam várias definições para alimentos funcionais não há nenhuma definição oficial que seja universalmente aceite, variando de acordo com a legislação de cada país (Martirosyan e Singh, 2015).
Por exemplo, a Legislação Europeia não contempla os alimentos funcionais como uma categoria de alimentos específicos, mas sim um conceito. No entanto, a definição que recentemente foi objeto de consenso científico foi a seguinte “um alimento pode ser considerado funcional se for demonstrado que o mesmo pode afetar beneficamente um ou mais funções alvo do corpo, para além de possuir os adequados efeitos nutricionais, de maneira que seja relevante tanto para o estado de saúde e bem-estar, como para a redução do risco de doença. Os alimentos funcionais devem ser
4 alimentos convencionais, que demonstrem os seus efeitos nas quantidades usualmente consumidas na dieta normal. Não se tratam de comprimidos ou cápsulas, mas sim alimentos normalmente incluídos nos padrões alimentares quotidianos” (EUFIC, 2015).
Em resumo, os alimentos funcionais possuem na sua composição, compostos bioativos, que ao serem introduzidos na dieta usual, modulam processos metabólicos ou fisiológicos, auxiliando na redução do risco de doenças crónicas não transmissíveis e na manutenção da saúde (Verschuren, 2002; Vidal et al., 2012). Exemplos de alimentos funcionais incluem os alimentos que contêm ingredientes funcionais específicos, que se encontram resumidos na Tabela 1.1. Entre as principais classes de ingredientes funcionais, estão os probióticos, vitaminas, minerais, antioxidantes, fitoquímicos, aminoácidos, proteínas e ácidos gordos (Martins et al., 2004; Marques et al., 2012).
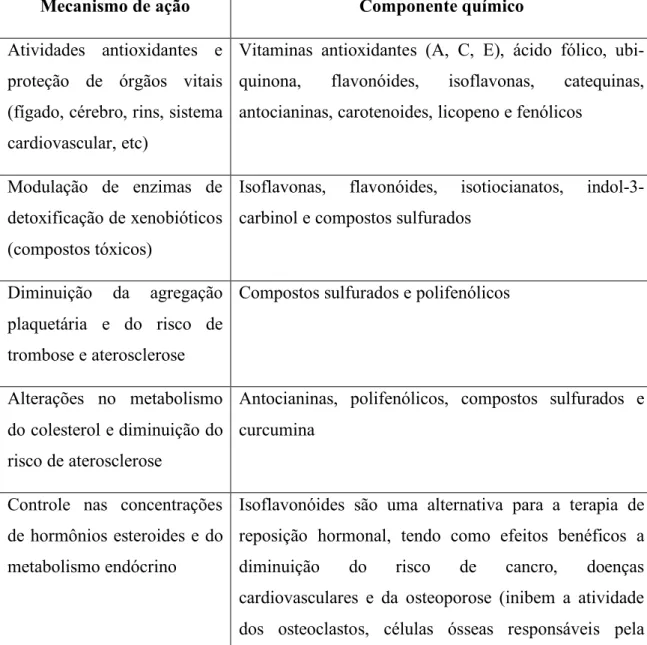
Tabela 1.1 - Componentes químicos envolvidos em alguns mecanismos de ações benéficos causados pela ingestão de alimentos funcionais.
Mecanismo de ação Componente químico
Atividades antioxidantes e proteção de órgãos vitais (fígado, cérebro, rins, sistema cardiovascular, etc)
Vitaminas antioxidantes (A, C, E), ácido fólico, ubi-quinona, flavonóides, isoflavonas, catequinas, antocianinas, carotenoides, licopeno e fenólicos
Modulação de enzimas de detoxificação de xenobióticos (compostos tóxicos)
Isoflavonas, flavonóides, isotiocianatos, indol-3-carbinol e compostos sulfurados
Diminuição da agregação plaquetária e do risco de trombose e aterosclerose
Compostos sulfurados e polifenólicos
Alterações no metabolismo do colesterol e diminuição do risco de aterosclerose
Antocianinas, polifenólicos, compostos sulfurados e curcumina
Controle nas concentrações de hormônios esteroides e do metabolismo endócrino
Isoflavonóides são uma alternativa para a terapia de reposição hormonal, tendo como efeitos benéficos a diminuição do risco de cancro, doenças cardiovasculares e da osteoporose (inibem a atividade dos osteoclastos, células ósseas responsáveis pela
5 reabsorção óssea)
Redução da pressão
sanguínea
Compostos sulfurados, potássio e dietas ricas em minerais e fibras
Efeitos antibacterianos e antivirais
Compostos sulfurados, especialmente a alicina (bactericida) e terpenóides
Atividades anti-inflamatórias Polifenólicos: inibem a produção de prostanóides, mediadores do processo inflamatório
Efeitos anticancerígenos Licopeno (cancro da próstata), resveratrol (potente indutor da morte de células tumorais), tocotrienóis (indutor da morte de células neoplásicas), fibras vegetais (diminuem a absorção de agentes indutores do cancro e aumentam a velocidade da digestão e excreção do bolo fecal
Proteção da visão contra a ação dos radicais livres, cataratas e degeneração macular
Luteína
Diminuição da absorção da glicose
Beta-D-glucanas (fibra alimentar)
Efeito antidepressivo e inibição do desejo de consumir álcool e dorgas ilegais
Ácidos clorogénios e melanoidinas
A indústria alimentar tem demonstrado interesse neste tipo de produtos alimentares encontrando-se atualmente disponíveis no mercado diversos produtos funcionais. São exemplos os alimentos enriquecidos com probióticos, como algumas bebidas de leite fermentado; os cereais de pequeno-almoço enriquecidos com minerais, fibras e vitaminas e os alimentos enriquecidos com ómega 3, como leite, pão, bolachas e ovos, entre outros (Siró et al., 2008).
6 O pão sendo um alimento de amplo consumo poderá ser um veículo importante de ingestão de ingredientes funcionais, dado que é possível incorporá-los durante a preparação do pão. Por exemplo, o pão pode ser enriquecido com cálcio, através da adição de sulfato, carbonato ou fosfato de cálcio sem afetar as propriedades reológicas da massa e as características do produto final ou ainda enriquecido com ómega 3 pela adição deste ácido gordo (Kajishima et al., 2003; Conto et al., 2012).
1.4 O Pão
É estimado que o pão tenha tido origem há 10 a 12 mil anos atrás na Mesopotâmia, juntamente com o cultivo do trigo. Os primeiros pães eram feitos de farinha misturada com o fruto do carvalho, eram achatados, duros, secos e muitos amargos e eram assados em rochas aquecidas pelo sol, e os grãos mais comuns para sua a fabricação eram a cevada e a espelta (espécies de trigo de qualidade inferior). O primeiro pão cozido em forno de barro foi a 7000 a.C. no Egito e para ser ingerido, o pão era lavado várias vezes em água a ferver e depois era assado sobre pedras ou por baixo de cinzas (Jacob, 2003).
Na Europa o pão chegou através dos gregos. O pão romano era feito em casa, pelas mulheres, tendo passado, posteriormente, a ser fabricado em padarias públicas, surgindo, então, os primeiros padeiros. Isto teria acontecido, segundo o filósofo romano Plínio, o Antigo, depois da conquista da Macedônia, em 168 a.C. (Vaz, 2004).
A partir do século XIX com a Revolução Industrial, os fornos movidos a gás substituíram os fornos de tijolo e de lenha, produzindo maior quantidade e qualidade de cocção de pães e massas em geral. As unidades automatizadas para elaboração de pães em grande escala aumentaram significativamente a produção de pães, tendo a França sido a pioneira, tornando-se assim o centro da panificação mundial.
Recentemente, a indústria de panificação adotou novas técnicas de panificação juntamente com a combinação de uma série de novos ingredientes para tornar o pão mais adequado às necessidades de uma dieta mais de acordo com os padrões atuais. Assim, devido à consciencialização crescente da população pela questão da alimentação saudável, a tendência da indústria de panificação é fabricar e promover o consumo de pão mais equilibrado, ideal para uma vida ativa e saudável, com pouco sal, pobre em gordura, constituído por cereais integrais e ricos em fibra e eventuais reforços de minerais e vitaminas (Dewettinck et al., 2008). O aparecimento de numerosos pontos de venda de “pão quente”, lojas em que pequenas quantidades de pão são confecionadas ao longo do dia de forma a corresponder às exigências do consumidor atual que tem uma
7 preferência por “um pão acabado de sair do forno, quente, aromático e crocante”. Para satisfazer esta exigência a indústria tem apostado no fabrico de massas congeladas ou já pré-confecionadas (Dewettinck et al., 2008).
Dependendo das matérias-primas usadas e da forma como são executadas as várias etapas do processo de fabrico, as características nutricionais do pão são variáveis, sendo, contudo, um alimento de elevado valor nutricional. É uma das maiores fontes de hidratos de carbono complexos, sob a forma de amido, da alimentação humana, sendo igualmente fonte de proteínas, fibras, lípidos, açúcares, minerais, vitaminas e aminoácidos (Vieira et al., 2007; Dewettinck et al., 2008).
1.4.1 Tipos de Pão
Segundo a legislação portuguesa, o pão é definido como – “o produto obtido da amassadura, fermentação e cozedura, em condições adequadas, das farinhas de trigo, centeio, triticale ou milho, estremes ou em mistura, de acordo com os tipos legalmente estabelecidos, água potável e fermento ou levedura, sendo ainda possível a utilização de sal e de outros ingredientes, incluindo aditivos, bem como auxiliares tecnológicos, nas condições legalmente afixadas” e “deverá revelar condições de fabrico normais e apresentar características organoléticas próprias, designadamente aroma, cor, sabor, textura de côdea, alveolado e consistência do miolo” (Decreto Lei 289/84).
De acordo, com o artigo 4º do DL 289/84 de 24 de Agosto, podem ser fabricados e comercializados os seguintes tipos de pão:
a) “Pão de trigo”, o pão fabricado com farinha de trigo dos tipos 45, 55, 65, 80 ou 110, água potável, sal e fermento ou levedura, podendo também ser utilizados glúten de trigo, extrato de malte e farinha de malte, açúcares e os aditivos referidos nos artigos 4.º e 5.º da presente portaria;
b) “Pão de centeio”, o pão fabricado com farinha de centeio dos tipos 70, 85 ou 130, ou em mistura com farinha de trigo dos tipos 45, 55, 65, 80, 110 ou 150, desde que a farinha de centeio seja utilizada numa incorporação superior a 50%, água potável, sal, fermento ou levedura, podendo também ser utilizados extrato de malte, farinha de malte, açúcares e os aditivos referidos nos artigos 4.º e 5.º da presente portaria;
c) “Pão integral”, o pão fabricado com farinha de trigo do tipo 150 ou com farinha de centeio do tipo 170, observando ainda o disposto nas alíneas a) e b), respetivamente;
8 d) “Pão de mistura”, o pão fabricado com mistura de farinhas de trigo dos tipos 45, 55, 65, 80, 110 ou 150, de centeio dos tipos 70, 85, 130 ou 170 e de milho dos tipos 70, 100 ou 175, ou apenas com farinhas de dois destes cereais, com uma incorporação mínima de 10% de farinha de cada cereal, água potável, sal, fermento ou levedura, podendo também ser utilizados glúten de trigo, extrato de malte, farinha de malte, açúcares e os aditivos referidos nos artigos 4.º e 5.º da presente portaria;
e) “Pão de milho” ou “broa de milho”, o pão de mistura cujo fabrico seja utilizada predominantemente farinha de milho dos tipos 70, 100 ou 175;
Segundo o mesmo diploma, no fabrico de pão especial é permitida a utilização dos seguintes ingredientes, estremes ou em mistura:
a) Leite inteiro, desnatado ou magro, pasteurizado, ultrapasteurizado, esterilizado, concentrado, condensado ou em pó, leitelho e soro de leite;
b) Manteiga;
c) Gordura e óleos comestíveis, margarinas e shortenings; d) Ovos, em natureza ou desidratados;
e) Preparados e enchidos de carne; f) Gérmen de trigo;
g) Sêmea e sêmola de trigo, de centeio ou de milho; h) Flocos de cereais;
i) Sementes comestíveis, em natureza; j) Farinha de leguminosa ou mandioca;
l) Fruta, em natureza, seca ou cristalizada, escorrida ou em calda; m) Alho, cebola ou tomate;
n) Especiarias, em natureza; o) Mel.
A nível nutricional, a qualidade do pão depende da taxa de extração da(s) farinha(s), dos cereais selecionados e do tipo de processamento utilizado (Cipriano, 2009). Há evidências científicas que consideram o pão um alimento funcional uma vez que pode atuar nos lípidos sanguíneos, na pressão arterial, no índice glicémico, no metabolismo da glicose e na sensibilidade à insulina (Sancho, 2005).
Hoje em dia, o pão está disponível num vasto leque de opções, para ir ao encontro das preferências e necessidades alimentares do consumidor. É o caso, por exemplo, do
9 pão meio sal, procurado especialmente por pessoas com hipertensão, e o pão sem glúten para cobrir as necessidades dos doentes celíacos, impedidos de consumir pão de trigo ou de outros cereais que possuam “glúten”. Em relação à variedade, só entre nós, basta pensar nos pães regionais que se fazem por todo o país, como a broa de Avintes, o pão alentejano, o pão de Mafra, a regueifa, não esquecendo os de inspiração francesa, como a baguete, pães de noz, passas ou sementes.
1.5 Caraterísticas e funções dos constituintes do pão
De uma forma geral, as matérias-primas básicas necessárias para produzir pão são: farinha, água potável, fermento e sal. No entanto, podem ser utilizados outros ingredientes na preparação do pão, que como referido anteriormente, encontram-se definidos na legislação. Em panificação os ingredientes dividem-se em dois grupos:
• Fundamentais: farinha, água, sal e fermento;
• Não fundamentais: açúcar, leite, gordura, enzimas e outros.
Cada ingrediente fundamental desempenha uma função específica na preparação do pão, como a seguir se descreve.
1.5.1 Farinha
Segundo o artigo 2º do DL 288/84, farinha define-se como o “produto resultante da moenda de grãos de cereais, maduros, sãos, não germinados e isentos de impurezas, destinado ao consumo humano” devendo seguir-se ao termo «farinha» a designação do cereal a que diz respeito.
O grão de cereal é constituído por três camadas principais: farelo, camada exterior designada comumente por casca, endosperma, porção intermediária e gérmen que é a semente, como se ilustra na Figura 1.
10
Figura 1- Composição de um grão de cereal.
A farinha é obtida pela moagem de grãos de cereal, que consiste na trituração do grão com o objetivo de se obter partículas com um tamanho mais adequado para as diversas aplicações industriais ou culinárias (Rodrigues, 2012).
Assim, durante o processo de moagem ocorre a separação do germe e a rutura do invólucro com a libertação do amido, que se encontra no endosperma, e a sua trituração numa poeira fina. Deste modo, o grão é transformado numa mistura de partículas de amido e de invólucro que é designada por farinha integral. Depois, esta mistura é submetida a um processo de peneiração, para separar o endosperma dos restos do invólucro ou farelo.
A nível da produção industrial de farinha são efetuados diversos tipos de peneiração, extraindo da farinha integral uma maior ou menor quantidade de farinha para consumo. De acordo com as taxas de extração conseguidas, isto é a percentagem de farinha que se obtém em relação ao peso total do grão, é possível conseguir vários tipos de farinha, designados de maior ou menor extração. Assim, quanto mais baixo for o grau de extração, mais branca é a farinha, contém cerca de 60-65 % do grão. As farinhas designadas de alto grau de extração (82-90 %) conservam a camada de aleurona e parte ou todo o escutelo, assim como a camada mais externa do endosperma. As farinhas de maior valor alimentar são as que possuem uma taxa de extração de 80-85 % e permitem ainda uma boa panificação (Ferreira, 1994).
As farinhas que podem ser usadas na indústria de panificação estão identificadas na Portaria nº 254/2003 e são as seguintes:
- farinhas de trigo – tipo 45,55, 65, 80, 110, 150; - farinhas de centeio – tipo 70, 85, 130, 170; - farinhas de milho – tipo 70, 100, 175.
11 Entre as farinhas de cereais usadas no fabrico de pão, a farinha de trigo é de longe a mais utilizada. A farinha de trigo é um produto obtido da principal espécie de trigo cultivada Triticum aestivum, e a sua composição é diferente de acordo com a região, as condições de cultivo e ano agrícola (OWENS, 2001). Na Tabela 1.2 apresenta-se os intervalos típicos da composição química do trigo (Pallarés et al., 2007). O trigo é o cereal mais usado na produção de farinhas panificáveis devido, essencialmente, à qualidade e quantidade de proteínas presentes que são capazes de formar o glúten e à quantidade de amido (Ribeiro, 2009).
Tabela 1.2 - Intervalo de variação da concentração dos principais componentes do trigo (Pallarés et al., 2007). Componentes Mínimo (%) Máximo (%)
Humidade 8,0 18,0 Amido 60,0 68,0 Proteína 7,0 18,0 Lípidos 1,5 2,0 Fibra 2,0 2,5 Cinzas 1,5 2,0
O glúten é formado pelas gliadinas, que são responsáveis pela viscosidade da massa, e pelas gluteninas, que conferem à massa a propriedade de resistência à extensão (Hoseney, 1994; Oliveira et al., 2009). Contudo a presença de outros constituintes, o amido, os lípidos e outros compostos hidrossolúveis são também determinantes para garantir o potencial de panificação, o qual é influenciado pelo teor e qualidade dos mesmos na farinha (Aquarone et al., 2001).
Na preparação do pão de trigo, quando a farinha é misturada com a água e é homogeneizada, verifica-se a hidratação das proteínas gliadina e glutenina que se associam, estabelecendo ligações por pontes de hidrogénio e ligações de Van der Walls, originando a formação da rede de glúten (Bobbio e Bobbio, 2001). Na Figura 2 apresenta-se um diagrama representativo da formação da rede de glúten.
Figura 1.2 - Diagrama representativo da formação da rede de glúten a partir da glutenina e gliadina (adaptado de Bobbio e Bobbio, 2001).
12 À medida que se desenvolve o glúten a aparência da massa sofre alterações significativas: se inicialmente se apresentava húmida a pegajosa com o tempo a massa fica com um aspeto mais firme, homogéneo, liso e enxuto. Pode-se ainda observar a formação de um filme elástico, que pode ser finamente esticado sem se romper. Assim, a formação do glúten na panificação é extremamente importante dada a sua capacidade de conferir elasticidade e consistência à massa, além de permitir a retenção do gás carbónico, formado durante a fermentação, suportando o aumento do volume observado. Adicionalmente, durante a cozedura é necessário que exista uma rede estrutural que seja flexível e bastante elástica e que seja também razoavelmente forte após o produto ser removido do forno. O glúten, desenvolvido a partir da farinha, é o principal responsável pelo carácter elástico das massas durante a cozedura e pela sua estrutura semi-rígida após a cozedura.
O amido é outro componente da farinha de trigo importante para a qualidade final do pão. O amido representa cerca de 70 % da farinha. Estruturalmente, o amido é um polissacarídeo é constituído por cadeias de glucose, que podem ter uma forma linear (amilose) ou ramificada (amilopectina), como se ilustra na Figura 1.3. A amilose é um polímero de cadeia linear com ligações glicosídicas α-1-4, enquanto a amilopectina é uma estrutura altamente ramificada formada por ligações glicosídicas α-1,4 e α-1,6 (Tester, et al., 2004).
Figura 1.3 - Estruturas químicas da a) amilose e da b) amilopectina.
O amido presente na farinha é responsável pelas propriedades de volume, humidade, consistência e textura do produto final.
1.5.2 Gelatinização do amido
A gelatinização do amido causa mudanças irreversíveis nas suas propriedades, como o inchamento dos grânulos, a perda da estrutura cristalina e a solubilização dos amidos (Silva, 2001). Para cada amido, tem-se uma faixa de temperatura de
13 gelatinização característica, correspondente ao ponto de máxima viscosidade do amido. Esse intervalo de temperatura é medido a partir do início do desaparecimento das zonas cristalinas do grão até ao seu fim, e é visível em microscópio com luz polarizada (Bobbio; Bobbio, 2001).
Quando o amido está presente em água fria, os grânulos incham ligeiramente, entre 10 a 20%, devido à difusão e absorção de água nas regiões amorfas, mas este inchamento é um processo reservivel ao serem desidratados. Contudo, quando os grânulos são aquecidos em água a uma temperatura superior, alcança-se um ponto onde os grânulos inchados apresentam um fenómeno irreversível, perdendo a ordem estrutural, consequência da fusão dos cristais. Porém, quando so grânulos se expandem, a amilose é lixiviada para a fase aquosa intergranular. Estas mudanças moleculares levam a um aumento significativo na viscosidade da amostra.
Em conjunto, a rutura da estrutura granular e o inchamento devido à hidratação e a solubilização das moléculas de amido, mostram o fim da gelatinização (Bello-Pérez; Montealvo; Acevedo, 2006; Tester & Morrison, 1990). As propriedades de gelatinização dos amidos são relacionadas a uma variedade de fatores, tais como: o tamanho, a proporção e tipo de organização cristalina, e a estrutura do grânulo de amido (Noda et al., 1998; Lindeboom et al., 2004).
1.5.3 Gelificação e retrogradação do amido
Após a gelatinização ou formação de pasta, as moléculas de amilose têm uma forte tendência a associarem-se através da formação de pontes de hidrogénio com outras moléculas de amilose adjacentes, isto ocorre quando a solução arrefece ou se mantém por um longo período de tempo. Ao arrefecer, a dispersão do amido gelatinizado converte-se numa pasta viscoelástica turva ou em concentrações de amido suficientemente altas (>6% p/p) num gel elástico e opaco. A amilose exsudada dos grânulos inchados forma uma rede, por associação das cadeias que rodeiam os grânulos gelatinizados. A gelificação do amido é determinante na qualidade de muitos processos alimentares (Bello-Pérez et al., 2006).
A retrogradação é um fenómeno complexo e depende de muitos fatores, como a fonte e concentração de amido, condições de aquecimento e arrefecimento, pH e presença de solutos como lípidos e açúcares. Essa consiste de dois processos separados, o primeiro refere-se à gelificação das moléculas exsudadas dos grânulos de amilose durante a gelatinização e a segunda à recristalização da amilopectina (Bello-Pérez; Montealvo; Acevedo, 2006).
14 Durante a gelitinização e a retrogradação ocorrem mudanças nos grânulos de amido que são os principais determinantes do comportamento da past desses amidos, as quais têm sido medidas principalmente pelas mudanças de viscosidade durante o aquecimento e arrefecimento de dispersões de amido usando equipamentos como o viscoamilógrafo Brabender ou Rápido Visco Analisador (RVA), que registam a alteração da viscosidade de um sistema amido-água, sob agitação, em relação à temperatura e tempo (Cereda et al., 2001). No viscoamilógrafo (RVA) durante a fase de temperatura constante (95ºC) os grânulos começam a quebrar e a solubilização dos polímeros contínua. Nesse ponto, ocorre uma redução ou quebra da viscosidade. Durante a fase de arrefecimento, os polímeros de amilose e amilopectina solubilizados começam a reassociar-se ocorre um aumento na viscosidade, conhecido como tendência à retrogradação (Matsuguma, 2006).
1.6 Água
A água tem um papel primordial na formação da massa, pois hidrata a farinha, assegurando a união das proteínas que dão origem à rede de glúten e ao mesmo atua como solvente e plastificante, permitindo que ocorra o fenómeno de gelatinização do amido durante o cozimento do pão (León e Rosell, 2007). A sua presença permite ainda criar as condições adequadas para a ação das enzimas da farinha e promove a dissolução do açúcar e do sal, com uma temperatura adequada, para não retardar o crescimento da massa ou destruir a levedura, caso esteja excessivamente fria ou quente (Lidon, 2007).
Devido às suas caraterísticas, consegue controlar a consistência da massa, bem como a sua temperatura, controla a maciez do pão, dissolve os sais, suspende e distribui os restantes ingrediente que não a farinha, intumesce e humedece o amido, tornando-o mais digerível e, possibilita a ação de enzimas (Goias, 2012).
No pão, a quantidade a adicionar está associada à capacidade de manipulação da massa durante o processo de fabrico do pão.No caso de se adicionar menor quantidade da que está estipulada, a massa obtida será firme e difícil de moldar e, consequentemente, obtêm-se pães com pouco volume e com fraca aparência externa. Se pelo contrário, se a adição de água for em excesso a massa flui com muita facilidade e é difícil de moldar, obtendo-se pães de má qualidade. A quantidade de água a utilizar é determinada pela qualidade da farinha, concretamente dos teores de proteínas e de amido. Farinhas provenientes de trigos fortes absorvem maiores quantidades de água que os trigos fracos.
15 O seu conteúdo contribui de forma decisiva para a qualidade e vida útil dos produtos de panificação (Rodrigues, 2012).
1.7 Sal
O sal sempre foi utilizado na panificação e contribui de modo positivo para o sabor do pão e um aroma mais intenso, como também controla a atividade de água (aw)
proporcionando maior tempo de vida útil no pão, mas também faz com que seja mais fácil processar o pão, pois o glúten torna-se mais rígido devido à formação de fibras curtas, tornando a massa mais compacta.
A sua adição permite uma maior resistência e capacidade de retenção de gases, uma vez que o sal normaliza a atividade do fermento, controlando assim a fermentação. Também melhora a hidratação da massa, sem torna-la pegajosa, e a cor do miolo fica favorecida (VITTI, 2001).
Segundo a Lei n.º 75/2009 de 12 de Agosto, referente à redução do teor de sal no pão, estabelece que o teor máximo de sal no pão é de 1,4 g por 100 g de pão pronto a consumir, ou seja, pão cozido.
1.8 Levedura
Levedura é o nome genérico dado a um grupo de organismos unicelulares que se situam entre os fungos, que se reproduzem por divisão celular, e que geralmente dispõem de capacidades enzimáticas, capazes de decompor produtos químicos complexos, principalmente açúcares, noutros mais simples (ACIP, 2015).
A função da levedura é a de produzir dióxido de carbono que contribui para a expansão da massa devido à formação de numerosos alvéolos no interior da mesma, percursores dos alvéolos do miolo do pão. Assim, as leveduras tornam a massa mais elástica e porosa, possibilitando obter um pão mais digestível e nutritivo. Nas padarias utiliza-se fermento fresco, da espécie Saccharomyces cerevisiae e a sua função principal é provocar a fermentação dos açúcares, produzindo dióxido de carbono e outros compostos que conferem ao pão o aroma e o sabor característico. Também se podem utilizar outras espécies de leveduras, como S. rosei, S. rouxii e S. delbrueckii, que são interessantes para fermentações de massas com elevado teor de açúcar ou para reforço do sabor (Cauvain e Young, 2006).
No início do processo fermentativo a levedura efetua um consumo rápido da sacarose, da glucose, e da frutose presentes na farinha, aumentando o teor de maltose,
16 devido à ação das α- e β-amilases da farinha. Após o desaparecimento desses açúcares, a fermentação da maltose tem início (Lidon, 2007).
A produção de dióxido de carbono faz com que a massa se expanda para que alcance o volume necessário, dando-lhe a estrutura carateristicamente esponjosa ao miolo. A formação do dióxido de carbono dá-se pela presença de diferentes açúcares fermentáveis presentes na farinha que a levedura pode utilizar. Estes açúcares podem ser monossacarídeos (açúcares simples como a glucose, a frutose ou a galactose, que podem ser assimilados diretamente pela célula) e dissacarídeos (açúcares mais complexos como a sacarose ou a maltose, que a levedura necessita de decompor previamente em açúcares simples para poder assimilá-los posteriormente).
Os efeitos da levedura no processo de panificação, especialmente na produção de dióxido de carbono, podem ser afetados por condições e circunstâncias alheias à própria levedura, por exemplo:
- quanto maior a temperatura durante a fermentação maior será a velocidade de fermentação, até alcançar o limite fisiológico das células (cerca de 48-50°C) ou temperaturas abaixo do limite dos 8-10°C que inibem quase totalmente a atividade fermentador;
- a presença de sal na massa é geralmente um retardador da atividade, embora estudos recentes sugiram que uma massa com um teor de sal inferior a 2% (em relação à farinha) fermenta mais rapidamente que uma massa sem sal (ACIP, 2015);
- a adição de ingredientes à massa que provoquem um aumento da sua pressão osmótica, como o açúcar em concentrações superiores a 8-10%, atrasam também a fermentação, exceto no caso de se utilizarem leveduras especialmente adaptadas a estas condições;
- a composição das farinhas em amílases e açúcares disponíveis, faz igualmente variar a atividade , pois maior quantidade de açúcares livres corresponde a uma maior produção de CO2 (ACIP, 2015).
1.9 Farinhas em estudo
Atualmente há uma maior consciencialização por parte da população sobre os efeitos da alimentação na saúde dos indivíduos. Várias organizações, entre as quais a Organização Mundial de Saúde, têm alertado e reforçado a importância de uma alimentação saudável para a manutenção da qualidade de vida e na prevenção de várias doenças crónicas, tais como, a obesidade, as doenças cardiovasculares e a diabetes (OMS, 2004).
17 Sendo o pão um alimento reconhecidamente essencial numa dieta saudável e largamente consumido pela população, este pode ser um veículo importante de ingestão de ingredientes funcionais, dado que é possível incorporá-los durante a preparação do pão como por exemplo através da incorporação de farinhas com alto teor nutricional e componentes funcionais.
1.9.1 Chia
A semente de chia (Salvia hispanica L.) provém de uma planta (Figura 1.4) oriunda do México e é considerada uma oleaginosa, devido ao seu alto teor de óleo (Ayerza e Coates, 2011). Estas sementes faziam parte da dieta dos Astecas e Maias, para aumentar a resistência física, mas também como planta medicinal (Vidacelerieo, 2012).
Figura 1.4 - Planta (a) e sementes (b) de chia (Tosco, 2004).
Trata-se de uma pequena semente de forma oval e de cor castanho-clara. Possuem uma quantidade significativa de ácidos gordos, cerca de 40% do peso total da semente, sendo quase 60% de ácido α-linolénico (ómega-3) e cerca de 20% de ácido linoleico (ómega 6), estando entre as plantas com os valores mais elevados de ácido α-linolénico, como a camelina (36%) e o linho (57%) (Ayerza e Coates, 2011). A presença destes ácidos na dieta favorece a diminuição da ocorrência de doenças cardiovasculares. A caracterização química das sementes também revelou um teor de proteínas elevado, cerca de 19-23% do peso total, sendo superior ao teor da maioria dos grãos tradicionalmente utilizados, incluindo o trigo (14%), o milho (14%), o arroz (8,5%), a aveia (15,3%) e a cevada (9,2%). Os principais aminoácidos essenciais presentes nas sementes de chia são a leucina, lisina, valina e isoleucina (Sandoval-Oliveros & Peredes-Lopez, 2012). As sementes de chia contêm ainda minerais, vitaminas e antioxidantes naturais como tocoferóis (238-427 mg/Kg) e polifenóis, sendo os principais, ácido clorogénico, ácido cafeico, quercetina e kaempferol (Ixtaina et al.,
18 2011), que protegem os consumidores de algumas doenças, entre as quais as doenças cardiovasculares e certos tipos de cancro.
O elevado teor de fibras da semente de chia (34,6%) pode também ter efeitos benéficos na saúde, pois pode aumentar a saciedade e diminuir o consumo de energia podendo minimizar os fatores de risco associados ao aparecimento de várias doenças crónicas, como a obesidade, doenças cardiovasculares e diabetes do tipo 2 (Olivos-Lugo et al., 2010).
Tradicionalmente, no México, as sementes de chia são misturadas nos cereais, iogurtes ou saladas, podendo comer-se algumas como um simples snack (Sandoval-Oliveros e Peredes-Lopez, 2012). As sementes de chia são utilizadas como suplementos nutricionais, bem como na fabricação de barras, cereais matinais e biscoitos nos Estados Unidos, América Latina e Austrália (Dunn, 2010).
O interesse em estudar a chia como possível aditivo para os alimentos está relacionado com as suas características químicas, nomeadamente o seu elevado teor de proteínas, antioxidantes, fibras e ácidos gordos polinsaturados que podem ter um efeito benéfico na prevenção de doenças e na melhoria do bem-estar da população.
1.9.2 Maçã
A maçã é um dos frutos mais apreciados e acessíveis em todo o mundo (Figura 1.5). As maçãs constituem uma das principais fontes de fitoquímicos na dieta humana pois contêm uma complexa mistura de compostos bioativos que têm ações benéficas para a saúde (Babar et al., 2011).
Este fruto é caracterizado pelo seu paladar agradável, ligeiramente ácido, devido ao pH entre 3,90 e 4,27, e sabor adocicado devido ao teor elevado de açúcares, nomeadamente frutose, galactose, sacarose, glucose e sorbitol (Feliciano et al., 2010).
A composição nutricional da maçã é muito diversificada, pois são conhecidas diversas espécies e variedades. No entanto é possível referir que as maçãs contêm cerca de 80 % de água, 10% de açúcar, 2-3% de fibras alimentares e o teor de proteína não ultrapassa 0,2% e o de lípidos 0,5%. Contém ainda uma quantidade significativa de minerais, nomeadamente o sódio e o ferro, mas contém também cálcio, magnésio, manganês e fosfóro (Lozano, 2006). A maçã apresenta ainda uma grande quantidade de vitaminas do complexo B e pequenas quantidades de vitaminas A e C.
Este fruto constitui ainda uma fonte importante de polifenóis, nomeadamente de flavonóides, na dieta ocidental e a sua atividade antioxidante está entre as mais elevadas quando comparada com a de outros frutos e legumes frequentemente consumidos (Mari
19 et al., 2010). Aliás, as propriedades nutracêuticas atribuídas à maçã são devidas à presença destes compostos. Os vários estudos realizados mostraram que os compostos fenólicos presentes na maçã são fundamentalmente flavanóis (catequinas e procianidinas) os quais representam cerca de 63-71% do total de polifenóis, mas também podem ser encontrados ácidos hidroxicinâmicos (p. ex. ácido clorogénico) em quantidades apreciáveis (1-31%) e flavonóis (2-10%). Os teores de polifenóis totais, que dependem grandemente da variedade da maçã, podem oscilar entre 66,2 mg GAE/100g de peso fresco e 420,5 mg GAE/100g de peso fresco no fruto inteiro (Vrhovsek et al.,2004; Imeh e Khokhan, 2002).
Em geral, os compostos mencionados estão fundamentalmente concentrados na casca, que representa cerca de 10% do peso da maçã, na polpa a concentração é bastante menor (Chinnici et al., 2004b).
Figura 1.5 - Maçã golden (a) e farinha de maçã (b). Fonte: 2014.
1.9.3 Quinoa
A Organização das Nações Unidas para a Alimentação e a Agricultura (FAO) declarou oficialmente o ano 2013 "O Ano Internacional da Quinoa" (FAO, 2013). A proposta partiu do governo da Bolívia e recebeu um forte apoio de inúmeros países de centro e sul-americanos. A quinoa é considerada pela FAO como um alimento com "alto valor nutritivo," e biodiversidade incrível. A quinoa permanece desconhecida para a maioria da população, especialmente as suas possíveis aplicações na confeção de alguns alimentos, mas a FAO espera que esta situação inverta, visto que é um alimento rico em nutrientes.
O nome científico para a quinoa é Chenopodium quinoa Willd. A sua cor pode ser branca, cinzenta, rosa, roxa ou vermelha dependendo da variedade (Figura 1.6). A semente da quinoa é considerada um "pseudocereal", termo que é geralmente utilizado para descrever os alimentos que não são gramíneas, mas ainda assim pode ser facilmente moído e transformado em farinha. Foi inicialmente cultivada no Equador, Peru, Bolívia e em algumas áreas da Colômbia, Chile e Argentina, mas o seu cultivo
20 está a estender-se a outros países, como França, Inglaterra, Suécia, Dinamarca, Holanda, Estados Unidos, entre outros (León e Rosell, 2007).
Figura 1.6- Planta (a) e grão (b) da quinoa (FAO, 2013).
São vários os fatores que fazem da quinoa um alimento funcional e ideal para uma alimentação saudável, principalmente para alguns consumidores (idosos, crianças, atletas de alto desempenho, celíacos e pessoas intolerantes ao glúten e lactose). A quinoa apresenta teores mais elevados de proteínas e maior equilíbrio na distribuição de aminoácidos essências do que outros cereais, tais como o arroz e o milho (Ascheri et al., 2002), é ainda considerada como fonte de minerais e vitaminas do complexo B (riboflavina). Além disso, possuí quantidades significativas de flavonóides e ácidos fenólicos (Gewehr et al., 2012).
A composição nutricional das sementes de quinoa, revelou concentrações de proteína a variar entre 7,47 e os 22,08%, com uma média de 13,81%. Foram identificados 10 aminoácidos essenciais na quinoa: lisina, isoleucina leucina, fenilalanina, tirosina, treonina, triptofano, valina, histidina e metionina. De acordo com os valores indicados pela FAO/WHO (WHO, 2002) a proteína presente na quinoa fornece 180% de histidina, 274% de isoleucina, 338% de lisina, 212% de metionina + cisteína, 320% de fenilalanina + tirosina, 331% de treonina, 228% de triptofano e 323% de valina da quantidade recomendada na fonte de proteína de um adulto. A quinoa apresenta também um teor em fibras alimentares elevado (superior a 6%, peso seco) quando comparado com outros cereais como o trigo e o arroz, que contêm cerca de 2,4% e 3,5%, respetivamente (Gewehr et al., 2012).
As sementes de quinoa são ainda uma fonte importante de amido, sendo o hidrato de carbono mais abundante, representando entre 58% a 64% do total de matéria seca, contendo cerca de 11% de amilose (Repo-Carrasco et al., 2003). Contém ainda outros açúcares, concretamente teores elevados de xilose e maltose e baixos teores de glucose e frutose. Num estudo realizado por Repo-Carrasco et al. (2003) foram obtidos os seguintes teores de açúcares: 1,79 mg/100g de glucose, 0,20 mg/100g de frutose, 2,90 mg/100g1 de sacarose e 1,40 mg/100g maltose.
21 A composição em minerais é também variada e rica, nomeadamente em cálcio, magnésio, fósforo, ferro e zinco (Repo-Carrasco et al., 2003; León e Rosell, 2007), embora os teores sejam significativamente afetados pela composição mineral da região, tipo de solo e aplicação de fertilizantes. Esta semente apresenta também um teor de lípidos apreciável, entre 1,8% e 9,5%, com um valor médio de 5,0%-7,2% (Vega-Gálvez et al., 2010). Num estudo realizado por Wood et al., (1993) obtiveram o valor de 5,3% para o teor de lípidos totais, dos quais 85% dos quais são ácidos gordos. Aproximadamente, 11% dos ácidos gordos são saturados predominando o ácido palmítico. Os ácidos linoleico, oleico e α-linolénico representam, respetivamente, 52,3%, 23,0 % e 8,1% do total dos ácidos gordos. Os autores referem ainda que a composição em ácidos gordos é semelhante à da soja. De realçar que apesar da elevada concentração o óleo mantem-se estável devido à grande quantidade de vitamina E que atua como antioxidante (Koziol, 1992; Repo-Carrasco et al., 2003). Com efeito, era espectável que a quinoa fosse mais suscetível à oxidação, devido ao elevado teor de lípidos, resultando assim uma diminuição dos nutrientes. No entanto, estudos recentes têm demonstrado que a quinoa não se oxida tão rapidamente quanto seria de esperar. Estes resultados são importantes do ponto de vista nutricional. Adicionalmente, o aquecimento, como a fervura e o cozimento, da quinoa não parece comprometer significativamente a qualidade dos ácidos gordos, o que permite apreciar a sua textura e sabor cozido, mantendo o benefício dos seus nutrientes. Os investigadores têm sugerido que é a matriz diversificada em antioxidantes, que inclui vários composto da família da vitamina E, como alfa, beta, gama e delta-tocoferol, assim como os flavonóides como a quercetina e miricetina que contribuem para esta proteção oxidativa.
Na quinoa podem-se encontrar também algumas vitaminas, concretamente ao ácido ascórbico (C), α-tocoferol (E), tiamina (B1), riboflavina (B2) e niacina (B3).
Vários autores têm dedicado também atenção à presença de antioxidantes. Pasko et al., (2009) mostraram qua as sementes, deste pseudocereal, contêm uma concentração elevada de antioxidantes, superior aos valores encontrados no amaranto, outro pseudocereal com propriedades nutritivas ímpares.
1.9.4 Linhaça
A linhaça, cujo nome científico é Linum usitatissimum L., é a semente de uma planta bem conhecida, o linho (Figura 1.7). A linhaça é uma oleaginosa e pode ser encontrada como grão, moída ou na forma de óleo. Embora haja registos do consumo desta semente, na Europa e na Ásia, desde 5000 a 8000 anos a.C., o seu consumo