MODÉLISATION DE LA QUALITÉ DU BIOGAZ PRODUIT PAR UN FERMENTEUR MÉTHANOGÈNE ET STRATÉGIE DE RÉGULATION. En revanche, peu d’études se sont concentrées sur la régulation de la qualité du biogaz.
Introduction
La découverte de la fermentation et du biogaz
Il faudra alors attendre 1776 et les vacances d'Alessandro Volta au bord du lac Majeur pour identifier le méthane, qu'il appelle gaz des marais ; lors d'une promenade en bateau, il a remarqué qu'en touchant le fond du lac avec un bâton, des bulles de gaz remontaient à la surface. Le terme méthane a été proposé pour la première fois en 1865 et finalement accepté en 1892 lors d'un congrès international sur la nomenclature chimique.
Un écosystème naturel complexe
C’est également à cette époque que sont formulées les premières équations macroscopiques de dégradation de la matière organique par fermentation méthanogène. 1.1 – Schéma de la chaîne trophique des étapes de fermentation (inspiré de Sinechal et al.
Microbiologie de la digestion anaérobie
- Hydrolyse
- Acidogénèse
- Acétogénèse
- Méthanogénèse
- Sulfato-réduction
De plus, les bactéries méthanogènes parviennent à rivaliser avec les homoacétogènes pour l'utilisation de H2 grâce à leur meilleure affinité pour ce substrat (Nollet et al., 1997). Ainsi, dans les environnements riches en composés soufrés, il peut y avoir compétition entre les bactéries homoacétogènes (BH), les bactéries méthanogènes (BM) et les BSR pour la dégradation de l'acétate et du dihydrogène (Visser et al., 1996).
Physico-chimie de la digestion anaérobie
- Température
- pH et alcalinité
- Les nutriments
- Composés toxiques ou inhibants la digestion anaérobie
Cependant, le rendement de purification dépend de la configuration du procédé et les rendements de croissance peuvent varier. La concentration seuil au-dessus de laquelle les AGV seront inhibiteurs dépend du pouvoir tampon du milieu.
Les procédés de digestion anaérobie
Généralités
- Avantages et limites de la digestion anaérobie
- Choix et dimensionnement d’un digesteur
La sonication (utilisation d'ultrasons) contribue également à favoriser la désintégration des composés solides. 1997) rapportent l'amélioration de la dégradation de la matière organique, et l'augmentation de la production de biogaz après l'utilisation des ultrasons. Le non-respect de cette limitation entraîne une réduction progressive de la biomasse dans le réacteur ; on parlera alors de lessivage.
Mode d’alimentation des réacteurs de fermentation
1.27) représente une limitation qui doit être respectée lors de la détermination de la taille du réacteur ; la technologie utilisée et les conditions appliquées doivent garantir un temps de séjour des solides supérieur au temps maximum de doublement des populations bactériennes. 1.27) Le non-respect de cette limitation entraîne une réduction progressive de la biomasse dans le réacteur ; on parlera alors de lessivage.
Solution technologies pour les bioréacteurs continus
- Les digesteurs à cellules libres
- Les digesteurs à biofilm et à granules
- Réacteurs à support mobile
- Réacteurs à deux étages
La récupération des particules du digestat peut se faire avec un décanteur ou une membrane. Une grande partie de la biomasse présente est en réalité coincée entre les interstices du support, plutôt que de le fixer.
Utilisation du biogaz
- Caractéristiques du biogaz
- Les modes de valorisation
- Valorisation thermique
- Valorisation électrique
- Co- et trigénération
- Biogaz véhicule et injection dans le réseau
- Contraintes pour la valorisation du biogaz
- Amélioration du débit de biogaz
- Purification du biogaz
- Elimination du sulfure de dihydrogène
- Elimination des composés organohalogénés, métaux lourds et siloxanes 49
- Elimination du gaz carbonique
- Traitement par biomasse autotrophe
Dans ce cas, le biogaz est brûlé dans une chaudière pour produire de la vapeur à haute pression. Le sulfure de dihydrogène présent dans le biogaz provient de la dégradation des protéines et d'autres composés soufrés.
Conclusion
- Le réacteur pilote
- Support de la biomasse
- Instrumentation
- Suivi du digesteur par des mesures hors-ligne
- Suivi du digesteur par des mesures en-ligne
- Planification expérimentale à l’aide de modèle
7.2) le dispositif est adapté pour permettre l'ajout de soude directement dans le digesteur au niveau de la boucle de recirculation, et non plus au niveau de l'alimentation (figure 2.3). La mesure du pH archivée correspond au signal de l'électrode pH placée au niveau de la boucle de recirculation.
Conclusion
Introduction
Il peut être utilisé pour reproduire ou expliquer un comportement observé, prédire un comportement, contrôler un système, etc. Cependant, un modèle n'est utile que s'il permet de répondre aux questions que l'on se pose sur le processus étudié. Un modèle est également caractérisé par un domaine de validité, où l'accord entre les valeurs de sortie du modèle et les mesures est satisfaisant par rapport aux objectifs fixés.
Le développement d’un modèle
Ceci explique pourquoi, parmi l'infinité de modèles valables, un modèle peut avoir un avantage sur les autres, car il apportera des réponses aux questions posées. A ce stade, de nouvelles données qui n'ont pas été utilisées pour l'identification doivent être utilisées.
Modèles de la digestion anaérobie
- Modèle cinétique enzymatique
- Du chemostat au méthaniseur
Andrews (1968) a suggéré d'utiliser une fonction Haldane (équation 3.1) pour représenter l'inhibition de la croissance du méthanogène à des concentrations élevées de substrat. Parallèlement, Ierusalimsky s'est intéressé à l'inhibition non compétitive de la croissance sur un substrat simple et a introduit l'équation (3.8) où I est la concentration de l'inhibiteur et Ki est la constante d'inhibition.
Modèle ADM1
Structure du modèle ADM1
Lors de nos recherches, nous avons utilisé différents modèles issus de la littérature, les modèles ADM1 et AM2, ainsi que le modèle AMH1, qui est une adaptation du modèle d'Andrews pour un processus à biomasse fixe (voir chapitre 6.4). Les sections suivantes présentent les modèles ADM1 et AM2, tandis que le modèle AMH1 sera abordé en détail dans la section 6.2.
Choix de modélisation
L'effet de la température, déjà pris en compte dans le modèle de Sinechal et al. 1979), est également une caractéristique du modèle ADM1 ; Cette dépendance en température des paramètres cinétiques et physico-chimiques permet d'ajuster le modèle pour représenter un processus mésophile ou thermophile. Le modèle de transfert choisi s'appuie sur la théorie des deux films (Graef et Andrews, 1974).
Modèle AM2
Présentation du modèle
Les auteurs ont favorisé ces différents choix de modélisation en raison de leur flexibilité, qui permet de retirer ou d'ajouter facilement de nouveaux substrats, des fonctions d'inhibition ou même des espèces pour tenir compte de la compétition pour l'accès aux substrats (par exemple, les réducteurs de sulfate) (IWA, 2005). Compte tenu du caractère très insoluble du méthane, les auteurs ont choisi de montrer uniquement le transfert de CO2 entre la phase liquide et la phase gazeuse.
Equations du modèle
La cinétique de croissance des bactéries acidogènes est représentée par l'équation de Monod (3.2), tandis que l'inhibition de la croissance des méthanogènes par de fortes concentrations d'AGV obéit à la cinétique de Haldane (3.1).
Discussion
Choix d’un niveau de description et complexité associée
Limites des modèles : la modélisation des transferts gazeux
Dans le cas d'un digesteur anaérobie, cette surface d'échange entre les phases liquide et gazeuse correspond à la surface totale des bulles formées dans le réacteur, à laquelle s'ajoute la surface libre de la colonne d'eau. Afin d'estimer la surface et ainsi calculer le coefficient kLa, nous avons mis en place un modèle de formation des bulles et d'évolution de leur taille au sein de la colonne d'eau.
Modèle de création et d’évolution des bulles dans un méthaniseur
- Equations d’évolution de la taille des bulles
- Equations de nucléation et détachement des bulles
- Débit molaire de CO 2 et coefficient k L a moyen
- Résultats et discussion
En raison des flux de CO2 et de l'évolution de la pression hydrostatique PL, le rayon d'une bulle va changer au cours de sa remontée. A partir des mesures du débit molaire de CO2 (qCO2) et de la pression partielle PC, nous estimons le coefficient de transfert macroscopique comme suit.
Modèle réduit d’échanges gazeux
Enfin, ce modèle complet ne permet pas d'identifier facilement les paramètres qui affectent le coefficientinkLa. Dans la section suivante, nous proposons de modifier le modèle AM2 en incluant l'équation (4.14) pour calculer le coefficientinkLa.
Résultats
Modification de l’équation de transfert liquide/gaz du modèle AM2 : le modèle
Le taux de kL dépend principalement du gaz, tandis que la surface varie avec la nature de la phase liquide et avec le débit de biogaz (Pauss et al., 1990 ; Merkel et Krauth, 1999). NC(z, z0)b(z0)dz0 (4.9) L'équation (4.9) permet également de calculer la pression partielle PCO2 en tête du digesteur à partir des débits de gaz qCOT 2 et qTCH4 et de la pression dans le réacteur à dôme.
Application aux données
Nous choisissons de remplacer l’équation du flux molaire qC dans le modèle AM2 par la nouvelle équation (4.15).
Discussion & Conclusion
Description des vinasses
Les tableaux 5.1, 5.2 résument les caractéristiques des échafaudages utilisés pour la première série d'essais (séries 1, 2 et 3). 5.2 – Caractéristiques des échafaudages utilisés lors des expérimentations des séries 2 (juillet 2005) et 3 (octobre 2005).
Alimentation synthétique et conditions opératoires
Le pH de l’alimentation intervient directement dans le calcul de l’alcalinité d’entrée, qui affecte la qualité finale du biogaz. 5.1 – Surface de réponse de la qualité du biogaz en fonction des caractéristiques de l'alimentation simulée à l'aide du modèle AM2.
Résultats
Calibration du modèle ADM1
Détermination des paramètres
Simulations & discussion
Par ailleurs, l'analyse des différences entre les points expérimentaux (Figure 5.2 b) et la surface simulée montre une bonne corrélation entre le modèle et les mesures ; les pourcentages de méthane observés sont conformes aux attentes. Cette alcalinité supplémentaire n’étant pas consommée dans le procédé, l’alcalinité du digesteur augmente logiquement (Figure 5.5 d), entraînant une augmentation du pH (Figure 5.5 b), ainsi que des bicarbonates et du carbone inorganique dissous (Figure 5.6 b, etc.).
Calibration du modèle AM2
Détermination des paramètres
- Paramètres de l’acidogénèse
- Paramètres de la méthanogénèse
- Interprétation des différences de paramètres
Nous avons choisi d'enregistrer le taux de croissance des bactéries acidogènes, µ¯1, et d'identifier le taux de biomasse libreα et la constante d'affinité KS1. Le taux de biomasse libre α est plus élevé pour la série 2 que pour la série 1.
Calibration du modèle AM2G
Comparaison des équilibres des modèles AM2 et AM2G
Comparaison des modèles AM2G/AM2
Discussion & Conclusion
Les capteurs pour les procédés de digestion anaérobie
Or, le démarrage d'un fermenteur est long (au moins 2 mois et presque 1 an pour les réacteurs thermophiles (Cresson, 2006)), mais conditionne par ailleurs le déroulement futur du procédé (Michaud et al., 2002). . L'utilisation d'une mesure directe des AGV comme variable clé semble plus importante et plus efficace pour garantir une bonne progression de la fermentation (Pind et al., 2003).
Des capteurs logiciels pour la digestion anaérobie
Par exemple, la méthode de spectrophotométrie infrarouge développée par Steyer et al. 2002a) permet la mesure de la DCO après un étalonnage strict de l'appareil. Pour remplir ces deux objectifs, l'équation (6.3) est souvent complétée par une structure d'observateur (Bernard et al., 2006b).
Utilisation de l’information pour le diagnostic des fermenteurs
Construction d’un indice de risque de déstabilisation d’un procédé de fermentation
- Présentation du modèle AMH1
- Etude du modèle
- Analyse de la dynamique du modèle
- Etude de stabilité des équilibres du modèle
- Conclusions et remarques
- Bassin d’attraction du point de fonctionnement normal et critère de stabilité
- Définition du bassin d’attraction et du critère de stabilité
- Calcul de l’indice de stabilité
- Marge de stabilité du procédé : un critère plus simple
- Comparaison entre l’indice de stabilité et la marge relative de stabilité 128
- Discussion
Comparaison entre l'indice de stabilité et la marge de stabilité relative 1286.2.5 Application de l'indice de risque à un processus réel. 129 6.3 Analyse dynamique du risque d'acidification dans un procédé de digestion anaérobie 1316.3.1 Division du plan de phases.
Analyse dynamique du risque d’acidification d’un procédé de digestion anaérobie
Partitionnement du plan de phase
Pour analyser qualitativement la dynamique du système (6.4), nous divisons le plan de phase en plusieurs régions où les variables sont de signe constant d'une manière similaire à Bernard et Gouzé (2002). Les tendances actuelles d'évolution du système ne permettant pas de positionner précisément le système, nous nous intéressons dans la section suivante à la dynamique du passage d'un domaine à un autre afin d'identifier la trajectoire du système. l'avion.
Dynamique d’évolution du système
Même avec des conditions initiales favorables, le système sera capable de traverser des zones proches du séparateur avant d'atteindre l'équilibre (voir Figure 6.10 a). De même, les zones en Λ† sont classées selon le nombre de transitions nécessaires avant d'atteindre la zone 14.
Suivi dynamique des trajectoires du système
6.13 – Exemples de trajectoires dans le plan de phase et les séries de transitions associées a) dans le bassin d'attraction utile, b) dans le bassin d'acidification. bassin utile, b) dans le bassin d'acidification.
Réduction des graphes de transitions
Evolution du plan de phase après un changement incrémental des conditions
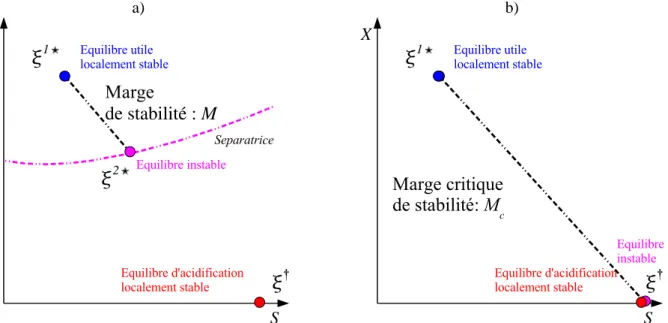
Nous définissons l'indice de stabilité IS comme la taille relative du bassin d'attraction d'équilibre ξ1 ? dans le domaine K\Λ ? (voir Figure 6.5). 6.6 – Définition de a) limite de stabilité, b) limite critique de stabilité dans le plan de phase.
Construction d’un indice de risque global
Le classement global obtenu est le suivant : de la zone la plus sûre (2) à la zone la plus dangereuse (14) pour la stabilité du procédé. La zone 14, en tant que zone de convergence du bilan d'acidification, est certainement la plus dangereuse.
Discussion & Conclusion
La zone 2 est considérée comme la plus sûre, car elle combine l'avantage d'être une zone de convergence vers l'équilibre normal de fonctionnement, et d'être suffisamment éloignée du séparateur pour qu'une augmentation de la charge organique ne risque pas de déstabiliser le procédé. Dans la section suivante, nous développons des observateurs pour estimer la biomasse et le taux de croissance à partir de la mesure du flux de méthane et de la DCO entrante.
Estimation des variables associées à la méthanogénèse
Construction d’un observateur asymptotique pour la biomasse méthanogène et
- Equation de l’observateur
- Application
La trajectoire qualitative du système dans le plan de phase est déterminée à partir des mesures de certaines variables (débit de méthane, DCO). A partir du suivi de certaines variables (par exemple le flux de méthane), nous essayons d'évaluer qualitativement la position du système dans le plan de phase.
Discussion
Dans la figure 6.22 a), nous avons présenté l'évolution du taux de croissance estimé et de l'AGV pour confirmer l'indice de risque (figure 6.22 b). 6.22 – Validation de l'indice de risque AGV (.) et du taux de croissance estimé (- -) pour une série d'expériences de surcharge organique.
Conclusion
Stabilisation du procédé autour d’une consigne
7.3 – Représentation schématique d'un contrôleur adaptatif. solution à appliquer en réacteur, Renard et al. 1988) ont pu ajuster la concentration du substrat au point de consigne souhaité. Par exemple, Guwy et coll. 1997) ont ajusté la concentration de bicarbonate dans un solvant à l'aide d'un réseau neuronal contrôlant une pompe à soude supplémentaire.
Optimisation du procédé
Concernant le contrôle automatique de la qualité du biogaz, Heinzle et al. 1993) citent des essais non concluants pour réguler la pression partielle en CO2 ou CH4 en ajoutant du liquide de refroidissement à l'aide de commandes numériques, ou en contrôlant le débit d'alimentation à l'aide d'une commande PI. Plus récemment, Holubar et al. 2002) ont tenté de combiner le traitement d'une charge maximale avec la production de biogaz à forte teneur en méthane, en agissant uniquement sur le taux de dilution.
Contrôle de la qualité
Analyse des expériences Série 1 et Série 2
Dans la suite de ce chapitre nous proposons d'étudier la possibilité de réguler la pression partielle de CO2 en contrôlant la concentration de CO2 dissous.
Contrôle de la pression partielle de CO 2 via le taux de dilution
- Equations du contrôleur
- Résultats
- Discussion
7.5 – Taux de dilution calculé par le contrôleur et CO2 dissous pour le scénario 1 ; a) contrôleur linéarisé, b) contrôleur asymptotique. linéarisation, b) contrôleur asymptotique. 7.6 – Qualité et débit du biogaz pour le scénario 1 dans le cas de a) linéarisation, b) contrôleur asymptotique avec le modèle AM2G. asymptotiquement avec le modèle AM2G. a).
Contrôle de la pression partielle de CO 2 via l’alcalinité
- Mise en place du dispositif de contrôle
- Contrôleur PI
- Contrôleur "mixte" modèle-PI
7.11 – Contrôle de la qualité du biogaz par un contrôleur PI : a) point de consigne et %CO2, b) débit d'alimentation appliqué. force appliquée. a). 7.13 – Régulation de la qualité du biogaz par un contrôleur PI : a) acides gras volatils, b) bicarbonates.
Conclusion & Discussion
Schéma de la chaîne trophique des étapes de la fermentation (inspiré de Sinechal et al
1.3 – Réactions d'acétogenèse avec production de dihydrogène et de formiate, et énergie libre associée (d'après Hall et al., 1992, Boone et al., 1989). Les paramètres cinétiques de croissance des bactéries sulfato-réductrices suggèrent qu'elles remplacent les bactéries méthanogènes, qui remplacent elles-mêmes les bactéries homoacétogènes, à de faibles concentrations de H2 (Weijma et al., 2002).
Effet de la température sur le taux de croissance des méthanogènes (extrait de IWA Task
Ces composants élémentaires doivent être présents dans le substrat selon les proportions de la formule empirique de la biomasse C2H7O2NP0.06S0.1 (Braun, 2007). Ces composés sont soit apportés par l'effluent, soit produits lors d'une des étapes de la méthanogenèse.
Comparatif des procédés anaérobie et à boues activées
En règle générale, la concentration des eaux usées à traiter n'est pas un paramètre limitant et les procédés anaérobies s'adaptent à des charges élevées (supérieures à 20 kgDCO.m-3). Selon la technologie utilisée pour le réacteur (voir section 1.4.3), cela sera lié différemment au temps de rétention des solides (TSS).
Schéma d’un digesteur infiniment mélangé : a) mécaniquement par pâles, b) par com-
Augmenter la quantité de biomasse dans le digesteur permet d'améliorer les performances du système et ainsi d'augmenter les débits entrants et sortants ou de réduire le volume de la cuve. Des technologies ont été développées pour découpler le temps de séjour hydraulique de celui des solides et favoriser l’accumulation de biomasse.
Schéma d’un digesteur à contact où la rétention est assurée par a) décanteur, b) mem-
La solution la plus simple consiste à mettre en place un système à la sortie du digesteur pour séparer la biomasse des eaux usées et faire recirculer la biomasse concentrée. Le réacteur est rempli d'un support inerte de nature différente (roche, verre, plastique, etc.) et qui peut se présenter sous différentes formes (lamelles, treillis, etc.), sur lequel la biomasse peut se développer.
Schéma d’un digesteur à lit fixe : a) à flux descendant, b) à flux ascendant. A : alimenta-
Le digesteur est rempli d'un petit support inerte sur lequel et à l'intérieur duquel la biomasse peut se développer (voir figure 1.7). Comme dans le cas des réacteurs à lit fixe, la biomasse peut rester piégée entre les supports (Hall et al., 1992).
Exemple de support mobile ; le Bioflow™
De plus, un manomètre permet de mesurer la pression dans le dôme du réacteur. Les modèles de décomposition anaérobie existants conduisent à un calcul complexe de la qualité du biogaz (ici exprimée par le pourcentage de CO2 dans le biogaz).
Schéma d’un digesteur à deux étages. A : alimentation, S : sortie, G i : composés gazeux. 39
Installations en cogénération : a) moteur alternatif, b) turbine à gaz, c) turbine à vapeur,
La rentabilité de ce mode de production dépend principalement de la composition du biogaz brut et de l’épuration requise. De leur côté, O'Keefe et al. 2000) ont montré que le lavage du biogaz par microaération de la phase liquide n'inhibait pas les bactéries méthanogènes, tout en donnant de bons résultats (biogaz contenant 90% de méthane).
Synoptique et photographie du réacteur pilote pour le traitement des vinasses de distille-
Ce réservoir de dilution se déverse dans le réservoir d'alimentation (200 L), où le pH de l'influent dilué est régulé au moyen d'une pompe doseuse reliée à un bidon de carbonate de sodium (NaOH) très concentré (30 à 50 %). La recirculation de la phase liquide du haut vers la base du digesteur est assurée par une pompe centrifuge dont le débit peut être réglé manuellement de 100 à 1000 L.h-1 (700 L.h-1 dans notre cas).
Représentation schématique du système de dilution
Ils sont reliés à un bassin de dilution par un système de canalisations de 60 m de long et 0,1 m de diamètre. Le digesteur est alimenté par une pompe péristaltique à débit contrôlable ; l'influent est mélangé à la phase liquide recirculée avant d'être injecté à la base du digesteur.
Schéma du principe de l’ajout de soude : a) pour réguler le pH d’alimentation, b) pour
Avec l'équation (4.16), le calcul de la qualité du biogaz dans le modèle AM2G est grandement simplifié par rapport à l'équation (3.19) pour le modèle AM2. La quantité de vinaigre à ajouter est calculée à partir de la DCO des eaux usées brutes pour obtenir les ratios DCO d'entrée et AGVin/DCO indésirable.
Principe d’un observateur
Si les entrées ou les paramètres du modèle ne sont pas connus avec précision, il n'est pas possible d'obtenir un observateur exact (systèmes 6.2 et 6.3). D'un autre côté, si les limites des incertitudes sont connues, il est possible de cartographier l'état du système à l'aide d'une paire d'observateurs (O+,O−).
Principe d’un observateur par intervalles
Nous utilisons ces observateurs pour identifier les paramètres du modèle Haldane pour le taux de croissance des bactéries méthanogènes. Dans ce cas, on revient à l’étude d’un système proche du système de Monod (3.3), et l’équilibre interne est globalement exponentiellement stable (g.e.s).
Solutions de l’équation µ(S) = αD
7.17 – Régulation de la qualité du biogaz par un contrôleur PI à linéarisation « mixte » : température dans le digesteur. Notre principal apport est sans doute la régulation de la qualité du biogaz par ajout de soude.
Trajectoires possibles dans le plan de phase : a) dans le cas 3, b) dans le cas 4
Domaine maximal pour les conditions initiales dans le domaine de définition K (cas 4.). 126
La figure 6.7 illustre la relation entre l'indice de risque IS calculé numériquement et la marge de stabilité réduite. La figure 6.8 montre l'évolution de certaines mesures au cours de cette expérimentation, ainsi que l'indice de risque.
Taux de dilution, AGV mesurés, pH et indice de risque pour une expérience en surcharge
Caractéristiques de l’alimentation pour une expérience en surcharge organique réalisée
6.8 - Taux de dilution, AGV mesurés, pH et indice de risque pour l'expérience de surcharge organique réalisée au LBE. 6.10 – Déstabilisation du système après surcharge hydraulique : a) Trajectoires dans le plan de phase (- -) sans perturbations, (-) avec perturbations, b) Indice de risque associé.
Déstabilisation du système suite à une surcharge hydraulique : a) Trajectoires dans le
Le plan de phase (S, égal à S = SM). Le tableau 6.2 montre que cette subdivision du plan de phase n'est pas suffisante pour distinguer catégoriquement chaque zone ; par exemple. les zones 5, 8 et 12 ont exactement la même signature, tandis que les zones 5 et 8 sont dans le bassin d'attraction pour le bilan utile et la zone 12 dans le bassin d'attraction pour le point d'acidification.
Graphes des transitions de trajectoires du système dans Λ 1? (figure du haut), Λ † (figure
6.13 – Exemples de trajectoires dans le niveau de phase et séquence de transitions associée a) dans le bassin d'attraction utile, b) dans le bassin d'attraction acidification.
Exemples de trajectoires dans le plan de phase et séquence de transitions associée a) dans
6.14 – Suivi dynamique des transitions dans le plan de phase pour deux trajectoires fictives avec des conditions initiales similaires (S0 en mmol.L−1, X0 en g.L−1) de part et d'autre de la séparatrice.
Suivi dynamique des transitions dans le plan de phase pour deux trajectoires fictives avec
6.15 – Séquences de transitions possibles en Λ1 ? (image du haut) et Λ† (image du bas) dans le cas d'une connaissance partielle de l'état.
Séquences de transitions possibles dans Λ 1? (figure du haut) et Λ † (figure du bas) dans le
Evolution du plan de phase : a) après une augmentation et b) après une diminution de la
Dynamique d’évolution des régions du plan de phase avec un changement incrémental
A chaque changement du point de consigne, le contrôleur parvient à ramener la qualité du biogaz autour de la valeur souhaitée. Enfin, nous avons complété notre gamme de procédures de surveillance par des stratégies de contrôle qualité du biogaz.
AGV (.) et taux de croissance estimé (- -) pour la série 1
AGV (.) et taux de croissance estimé (- -) pour la série 2
AGV (.) et débit de méthane (o) pour la série 1
AGV (.) et débit de méthane (o) pour la série 2
Indice de risque pour les expériences de la série 2
7.12 – Régulation de la qualité du biogaz par un régulateur PI : a) débit total de gaz, b) pH dans le circuit de recirculation. boucle de recirculation. 7.16 – Régulation de la qualité du biogaz par un régulateur linéariseur-PI « mixte » : a) acides gras volatils, b) bicarbonates. instable, b) les bicarbonates.
Représentation schématique d’un système de contrôle manuel par un expert
Représentation schématique d’un système de contrôle automatique
Représentation schématique d’un contrôleur adaptatif
Par exemple, Costello et coll. 1989) ont proposé de réguler la concentration S du substrat en ajoutant un terme intégral à un régulateur de linéarisation selon l'équation. A partir de simulations, ces auteurs ont montré que cette approche était plus efficace que le contrôleur de Renard et al. 1988), sous l’hypothèse d’une mesure erronée du flux de méthane.
Deux scenarii de profils d’alimentation pour la simulation de stratégies de contrôle
Dans les deux cas, l’alcalinité de l’influent est calculée à partir de la concentration en AGV et en carbone inorganique dans l’alimentation. 7.5 – Taux de dilution calculé par le contrôleur et CO2 dissous pour le scénario 1 ; a) contrôleur linéarisé, b) contrôleur asymptotique.
Taux de dilution calculé par le contrôleur et CO 2 dissous pour le scénario 1 ; a) contrôleur
Qualité et débit du biogaz pour le scénario 1 dans le cas d’un contrôleur a) linéarisant, b)
Taux de dilution calculé par le contrôleur linéarisant et CO 2 dissous pour le scénario 2
7.15 – Régulation de la qualité du biogaz avec un régulateur PI à linéarisation « mixte » : a) débit total de gaz, b) pH dans la boucle de recirculation. gaz, b) pH dans la boucle de recirculation. a). La prise en compte de la dynamique de l'alcalinité permet d'actualiser la consigne en fonction de l'état réel du procédé, ce qui garantit une meilleure régulation.
Variations du débit pour la simulation d’un contrôleur PI pour piloter la qualité du biogaz. 161
Régulation de la qualité du biogaz par un contrôleur PI : a) débit total de gaz, b) pH dans
7.12 – Régulation de la qualité du biogaz par un régulateur PI : a) débit total de gaz, b) pH dans le circuit de recirculation. a).
Régulation de la qualité du biogaz par un contrôleur PI : a) acides gras volatils, b) bicar-
Les variations autour du point de consigne sont très nettement réduites comme le montre le tableau 7.3 qui combine les erreurs d'ajustement moyennes et les écarts types pour les deux stratégies de contrôle. Dans le cas du contrôleur PI, l'erreur moyenne est positive, tandis que le contrôleur mixte a tendance à ajuster le %CO2 légèrement en dessous du point de consigne.
Régulation de la qualité du biogaz par un contrôleur "mixte" linéarisant-PI : a) consigne
Les légères fluctuations du débit de gaz (Figure 7.15) peuvent être attribuées au contrôle difficile de la température lors de nos expériences, comme le montre la Figure 7.17. 7.15 – Régulation de la qualité du biogaz avec un régulateur PI à linéarisation « mixte » : a) débit total de gaz, b) pH dans la boucle de recirculation.
Régulation de la qualité du biogaz par un contrôleur "mixte" linéarisant-PI : a) débit total
Régulation de la qualité du biogaz par un contrôleur "mixte" linéarisant-PI : a) acides
Régulation de la qualité du biogaz par un contrôleur "mixte" linéarisant-PI : température
L'utilisation d'acide et de soude permettrait de réduire, lorsque cela est nécessaire, l'alcalinité pour obtenir la qualité de biogaz souhaitée. Le recours croissant à la méthanisation s’inscrit donc dans une politique de développement durable.
Indice de risque d’acidification pour une expérience en surcharge
Régulation de la qualité du biogaz par un contrôleur "mixte" linéarisant-PI
Produits de la dégradation du glucose
Selon le groupe de travail de l'IWA pour la modélisation mathématique des processus de digestion anaérobie (2002), la réaction 1.1 ne sera jamais observée et la production couplée de propionate et d'acétate selon la réaction (1.5) du tableau 1.2 devrait être prise en compte.
Fermentation hétéroacide (propionate et acétate) du glucose (Zeikus, 1980)
Cette phase utilise un groupe de bactéries appelées OHPA (Obligate Hydrogen Producing Acetogens), qui produisent de l'acétate et de l'hydrogène à partir d'acides C3+. Ces organismes ont été initialement démontrés par Stadtman et Barker (1951) qui, à l'aide de cultures pures, ont découvert deux bactéries méthanogènes qui dégradent les acides gras volatils par β-oxydation, qu'ils ont nommées Methanobacterium propionicum et Methanobacterium suboxydans.
Réactions d’acétogénèse avec production de dihydrogène et de formate, et énergie libre
Hall et coll. 1992) et Cresson (2006) rapportent des temps de doublement de l'ordre de 0,23 jour-1 pour Syntrophomonas wolfei et de l'ordre de 0,1 jour-1 pour Syntrophobacter wolnii. Le terme homoacétogènes fait référence à des bactéries strictement anaérobies qui produisent principalement de l'acétate et peuvent également utiliser le CO2 (équation 1.13) comme accepteur final d'électrons (Buschhorn et al., 1989).
Homoacétogénèse lithotrophe
De nombreux auteurs ont ainsi montré que l'ajout d'un inhibiteur spécifique de la méthanogenèse dans les cocultures syntrophiques inhibait complètement la dégradation du propionate et du butyrate (McInerney et al., 1981 ; Ahring et Westermann, 1987b ; Liu et al., 1999). Leurs expériences ont également mis en évidence le rôle inhibiteur du dihydrogène dans les réactions d’acétogenèse ; l'ajout d'excès de H2 au milieu de coculture a pour effet de stopper la dégradation du propionate et du butyrate, entraînant l'accumulation de ces deux composés.
Homoacétogénèse fermentative
Ces organismes peuvent produire du méthane à partir de divers substrats contenant un groupe méthyle, tels que l'acétate, le méthanol ainsi que les (n)-méthylamines (Hippe et al., 1979 ; Nishio et al., 1984). Dans une coculture de ces deux espèces, celle qui croît plus lentement à faibles concentrations (Methanosarcina) devra utiliser d'autres substrats comme le méthanol ou les méthylamines (Westermann et al., 1989).
Les bactéries hydrogénotrophes contribuent au reste de la production de méthane (environ 30 %) en réduisant le couple H2/CO2 ou en le formatant en méthane (Schmidt et Ahring, 1993). Toutes les bactéries méthanogènes sont capables de réduire le H2/CO2, mais seules certaines espèces dégradent également le formiate.
Réactions nettes de la méthanogénèse syntrophe à partir du propionate et du butyrate
Les bactéries sulfato-réductrices (SRB) sont capables de tirer leur énergie d'un grand nombre de substrats, dont l'hydrogène moléculaire (Akagi et Jackson, 1967). Comme accepteur final d'électrons, ils utilisent des sulfates (SO2−4), ainsi que des sulfites (SO2−3) et des thiosulfates (S2O2−3), qu'ils réduisent en sulfure (S2−) lors de la respiration anaérobie.
Des composés toxiques et inhibiteurs peuvent être responsables de mauvaises performances de méthanisation de l'effluent, voire dans certains cas bloquer le procédé, ce qui peut nécessiter l'arrêt et le redémarrage du digesteur. Ils ont été développés pour combiner les avantages des méthaniseurs à biomasse fixe (taux de rétention de biomasse élevés permettant des débits d'alimentation élevés) et ceux à cellules libres (faible risque de colmatage et bonne homogénéité du milieu).
Comparatif des différentes technologies des fermenteurs
Le gaz produit lors de la première étape contient majoritairement du CO2 (environ 70 %), et la présence de méthane peut résulter du choix de conditions opératoires n'excluant pas strictement les bactéries méthanogènes. Le choix d'un réacteur de méthanogenèse plus grand que le réacteur d'acidogénèse permet un taux de dilution plus faible dans la deuxième étape et est donc plus favorable à la croissance du méthanogène.
Composés à éliminer par traitement selon le mode de valorisation du biogaz
La cogénération permet la production d'énergie de travail (électrique ou mécanique) et d'énergie thermique. L'énergie mécanique est produite par un moteur (figure 1.10 a) ou une turbine (figures 1.10 b, c et d), et au lieu de perdre de l'énergie thermique vers une tour de refroidissement, la chaleur est récupérée ; il peut être utilisé par exemple pour chauffer des fermenteurs méthanogènes, sécher des digestats, produire de l'eau chaude ou alimenter un système de chauffage ou de climatisation.
Comparatifs des solutions en cogénération
Améliorer la production de biogaz, en termes de débit, commence par une bonne gestion du procédé. Il peut être intéressant de répondre à d'autres paramètres opérationnels comme le pH, la température ou encore le temps de séjour hydraulique et le temps de séjour de la biomasse (Yadvika et al., 2004).
Techniques de purification du biométhane
L'effluent est échantillonné à la sortie de la colonne d'ultrafiltration au niveau du détournement vers les analyseurs en ligne. Cela permet d'éviter la centrifugation des échantillons pour éliminer les composés insolubles dans la plupart des mesures.
Mesures pour le suivi analytique du fermenteur pilote et méthodes associées
Monod a également formulé le principe selon lequel le taux de croissance d'une population bactérienne peut toujours être représenté comme le produit de la biomasse vivante, le deuxième facteur étant le taux de croissance (Monod, 1942). L'inclusion des étapes d'hydrolyse et de solubilisation permet par exemple la représentation du recyclage de la biomasse morte ou l'interconnexion du modèle ADM1 avec un modèle à boues activées (Rosen et al., 2006 ; Volcke et al., 2006).
Différences de complexité des modèles ADM1 et AM2
Dans le chapitre suivant, nous cherchons à développer un modèle général de digestion anaérobie ayant des propriétés similaires au modèle AM2, mais où le calcul de la qualité du biogaz serait plus simple. LekLa diminue également avec le rayon moyen de la bulle rB, caractéristique comparable à l'influence de la tension superficielle σ dans le modèle mécaniste ; nous avions établi qu'une tension superficielle élevée entraînait un petit rayon pour les bulles de gaz et donc un coefficient de transfert plus faible.
Définition et ordre de grandeur des paramètres et variables du modèle
Paramètres du modèle simplifié de coefficient de transfert liquide/gaz
Les caractéristiques des étals peuvent varier selon l'origine, l'âge ou encore les conditions de stockage. Il n'est pas rare que le réservoir de stockage alimentant le réservoir de dilution soit changé au cours de l'expérience, et la composition du résidu brut doit être surveillée régulièrement pour ajuster le système de dilution aux conditions souhaitées.
Caractéristiques des vinasses utilisées au cours de la série 1 d’expériences (avril 2005)
Caractéristiques des vinasses utilisées au cours des expériences de la série 2 (juillet 2005)
Qualité théorique du biogaz produit selon l’équation de Buswell
En utilisant le modèle AM2 et les paramètres donnés dans Bernard et al. 2001), nous avons calculé la qualité du biogaz pour un ensemble de conditions opératoires (pHin,AGVin/DCOin) - voir Figure 5.1. Le tableau 5.4 résume les lignes directrices utilisées pour le pH des aliments, la charge organique (DBO) et le rapport AGV/DBO.
Récapitulatifs des conditions opératoires appliquées
En effet, le taux α et la constante KS1 reflètent d'une certaine manière l'âge du digesteur et l'adaptation des bactéries à leur environnement. Au chapitre 6.4 (p. 141) nous présentons une méthode d'estimation en ligne du taux de croissance des bactéries méthanogènes, basée sur la mesure du flux de méthane.
Paramètres de calage du modèle AM2 pour les séries 1 et 2
A partir de l'étude des bilans d'un modèle simple, nous construisons un indice de risque chargé d'évaluer le mode de fonctionnement, c'est-à-dire si de petites perturbations conduisent à une acidification du milieu. La méthode présentée par Genovesi et al. 1999) identifie différentes classes de défaillances, au niveau du capteur, au niveau de l'actionneur ou au niveau de l'étage biologique. 2004) ont également développé un système expert basé sur la logique floue pour suivre l'acidification d'un fermenteur méthanogène.
Stabilité des équilibres selon les paramètres opératoires
Ainsi, nous montrons que MRS (m) est une très bonne approximation de l’indice de stabilité IS. Cela est particulièrement vrai pour le jour 5 de la figure 6.8, où l'indice de risque est le plus élevé, alors que la concentration en AGV ne semble pas préoccupante.
Signature qualitative des régions du plan de phase
En supposant que le paramètre k6 soit parfaitement connu, le système (6.17) permet d'estimer à la fois le taux de croissance µˆ et la concentration de la biomasse ex.ˆ. Pour compenser les informations manquantes, il est alors possible d'utiliser des estimateurs de taux de croissance et de biomasse.