Rev. Bras. Reumatol. vol.57 número6
Texto
Imagem

Documentos relacionados
Avaliar a resposta terapêutica ao pamidronato no ganho de densidade mineral óssea da coluna vertebral e fêmur total em um grupo de mulheres pós-menopáusicas com osteopo- rose,
The multivariate analysis of the BMD gain in spine and femur in each time point, as a dependent variable, and age, PTH, fracture risk, and the annual dose of pamidronate
Objective: To assess esophageal involvement (EI) in juvenile localized scleroderma (JLS) population and the possible association between this gastrointestinal manifestation
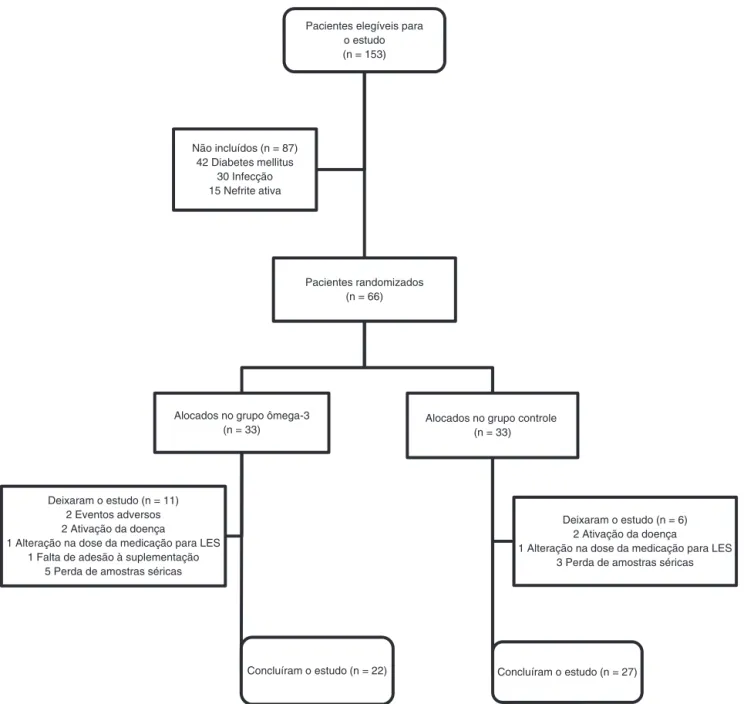
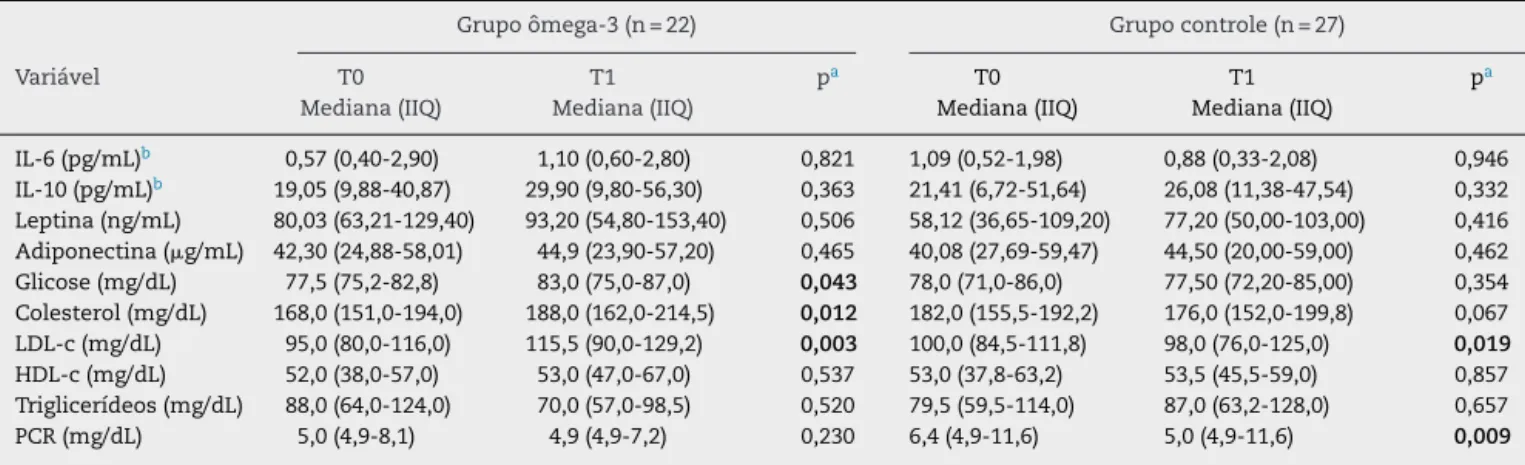
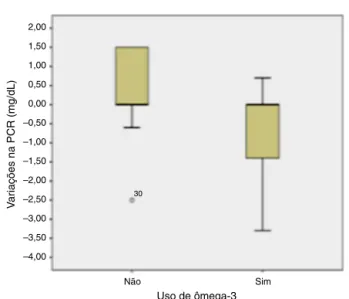
In conclusion, in this 12 weeks study in low disease activity lupus patients, the supplementation with omega-3 fatty acids was not associated with changes in serum levels of
Não houve diferenc¸a significativa na mediana da sobrevida renal entre os grupos de desfecho bom e ruim (p = 0,976) ( fig. Também não houve diferenc¸a significativa
present study, age, gender distribution, systolic blood pres- sure, BMI, serum albumin, creatinine, UPE (proteinuria in nephrotic ranges), eGFR (stages of chronic kidney
doenc¸a, durac¸ão das dificuldades, tratamento atual e período de tempo decorrido desde o início dos sintomas até o início do tratamento atual para a AR com o nível de
Demographic, socioeconomic and psychosocial factors, along with contextual and treatment factors, can largely explain the appearance of the high level of depression and fatigue and