UNIVERSIDADE DO ESTADO DE SANTA CATARINA – UDESC CENTRO DE CIÊNCIAS TECNOLÓGICAS – CCT DEPARTAMENTO DE ENGENHARIA MECÂNICA –DEM
PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIA E ENGENHARIA DE MATERIAIS - PGCEM
PRICYLA CORRÊA
SÍNTESE E CARACTERIZAÇÃO DE NANOCOMPÓSITOS HA/Al2O3-α SOL-GEL PARA APLICAÇÕES NA
RECONSTRUÇÃO ÓSSEA
JOINVILLE / SC
PRICYLA CORRÊA
SÍNTESE E CARACTERIZAÇÃO DE NANOCOMPÓSITOS HA/Al2O3-α SOL-GEL PARA APLICAÇÕES NA
RECONSTRUÇÃO ÓSSEA
Dissertação apresentada para obtenção do título de Mestre em Ciência e Engenharia de Materiais da Universidade do estado de
Santa Catarina, Centro de Ciências Tecnológicas - CCT
Orientador: Prof. Dr. Nelson Heriberto Almeida Camargo.
JOINVILLE / SC
C824s
Corrêa,Pricyla
Síntese e Caracterização de Nanocompósitos HA/Al2O3-α sol gel para Aplicações na Reconstrução Óssea / Pricyla Corrêa. – 2013.
134 p. : il. ; 21 cm
Orientador: Nelson Heriberto Almeida Camargo Bibliografia: p. 126-134
Dissertação (mestrado) – Universidade do Estado de Santa Catarina, Centro de Ciências Tecnológicas, Mestrado em Ciência e Engenharia de Materiais, Joinville,2013.
1. Ciência dos Materiais 2. Cerâmica 3.
Biomateriais 4. Nanoestrutura II. Camargo, Nelson Heriberto Almeida III. Universidade do Estado de Santa Catarina. Programa de pós-graduação em Ciência e Engenharia de Materiais IV.Título
Aos meus pais Doracilda e Jair que sempre incetivaram meus estudos.
AGRADECIMENTOS
Ao Prof. Dr. Nelson Heriberto Almeida Camargo, que como professor, orientador e amigo, jamais mediu esforços em me auxiliar, oferecendo sua enorme bagagem de conhecimento, dando condições para a realização deste trabalho;
À Universidade do Estado de Santa Catarina – UDESC e ao Programa de Pós-graduação em Ciência e Engenharia de Materiais - PGCEM pela infraestrutura oferecida;
À CAPES pela bolsa de mestrado;
Aos amigos do grupo de biomateriais Daiara Floriano da Silva, Gisele Maria Leite Dalmônico, Priscila Ferraz Franczak, Nelson Levandowski, Laís Passoni, Rafael Prandi, Cleomar Copatti e Mônica Schneider, que percorreram esta jornada comigo, sempre dispostos a ajudar;
Aos professores presentes na banca pela atenção e colaboração dada ao trabalho;
Ao meu companheiro Denilson Toneto da Silva pela paciência, apoio e incentivo;
Aos meus pais Jair Corrêa e Doracilda Corrêa que sempre incentivaram e apoiaram o desenvolvimento de meus estudos;
RESUMO
CORRÊA, Pricyla. Síntese e Caracterização de Nanocompósitos HA/Al2O3-α sol-gel para Aplicações na Reconstrução Óssea, 2013.
143 f. Dissertação (Mestrado em Ciência e Engenharia de Materiais – Área: Cerâmica) – Universidade do Estado de Santa Catarina. Programa de Pós Graduação em Ciência e Engenharia de Materiais, Joinville, 2013.
As biocerâmicas nanoestruturadas de fosfatos de cálcio se apresentam como biomateriais de reparação de defeitos e da reconstrução do tecido ósseo. Dentre os fosfatos de cálcio a hidroxiapatita é o biomaterial que mais apresenta similaridade com a estrutura cristalina do tecido ósseo, também oferece boa bioatividade e biocompatibilidade. A hidroxiapatita se destaca nas pesquisas como matriz óssea sintética e na elaboração de biomateriais nanocompósitos. O interesse na elaboração de biomateriais nanocompósitos está associado às propriedades mecânicas, modificação da morfologia, da arquitetura microestrutural, da área superficial de grãos e de microporos. Outro fator a ser levado em consideração está relacionado a melhorar a porosidade aberta e a capacidade de molhabilidade e capilaridade. O presente trabalho de pesquisa teve como objetivo a síntese via úmida de uma matriz óssea de fosfato de cálcio nanoestruturada para posterior elaboração da matriz hidroxiapatita e dos nanocompósitos hidroxiapatita/alumina-α sol-gel nas concentrações de 1, 2, 3 e 5% em volume de alumina-α nanométrica. O método de síntese para a obtenção da hidroxiapatita deu-se pelo processo de dissolução/precipitação, envolvendo fase sólida/líquida de CaO e ácido fosfórico. Este método permitiu a obtenção de pós nanoestruturados de hidroxiapatita formados por finas partículas aglomeradas. A elaboração dos pós nanocompósitos foi realizada com ajuda de um moinho atritor de alta energia. Os pós de todas as composições foram então compactados e sinterizados à 1250°C/2h fornecendo os biomateriais nanocompósitos HA/Al2O3-α. Os
partículas por laser, e cálculo teórico da área superficial das partículas para os pós nanoestruturados. Determinaram-se também as propriedades mecânicas, porosidade aberta e densidade hidrostática pelo método teórico para as diferentes composições de biomateriais obtidos da sinterização a 1250°C/2h.
ABSTRACT
CORRÊA, Pricyla. Synthesis and Characterization of HA/α -Al2O3 sol-gel Nanocomposites for Applications in Bone Reconstruction, 2013. 143 p. Dissertation (Master degree in Material Science and Engineering – Ceramics) – Universidade do Estado de Santa Catarina. Programa de Pós Graduação em Ciência e Engenharia de Materiais, Joinville, 2013.
Calcium phosphate nanostructured bioceramics present themselves as biomaterials for bone tissue reconstruction. Among calcium phosphates, hydroxyapatite is the biomaterial with the closest resemblance of bone tissue crystalline structure, also presenting good bioactivity and biocompatibility. Hydroxyapatite stands out on researches as synthetic bone matrix and in the making of nanocomposite biomaterials. The interest in the elaboration of nanocomposite biomaterials is associated with their mechanical properties, morphology modification, microstructural architecture, grain‟s surface area and microporosity. Another factor to consider is related to improving open porosity, wettability and capillarity. This research aimed at the wet synthesis of a nanostructured calcium phosphate bone matrix for later elaboration of the hydroxyapatite matrix and hydroxyapatite/α-alumina sol-gel nanocomposites at 1, 2,
3 and 5% concentrations in nanometric α-alumina volume. The
synthesis method for obtaining hydroxyapatite was the dissolution/precipitation process, involving liquid/solid CaO phase and phosphoric acid. This method allowed the obtainment of hydroxyapatite nanostructured powders composed of fine agglomerated particles. The elaboration of the nanocomposite powders was accomplished with the aid of a high-energy attrition mill. The powders of all compositions were then compacted and
sintered at 1250ºC/2h, supplying HA/α-Al2O3 nanocomposite
surface area for nanostructured powders) characterization. Mechanical properties, open porosity and density by theoretical method for the different biomaterial compositions obtained from sintering at 1250ºC/2h have also been determined.
LISTA DE ABREVIATURAS
ABNT – Associação Brasileira de Normas Técnicas ATD – Análise Térmica Diferencial
DRX – Difratometria de Raios X
FTIR – Epectroscopia de Infravermelho pó Transformada de Fourier HA – Hidroxiapatita Estequimétrica
JCPDS – Joint Committee on Powder Diffraction Standards MEV – Microscopia Eletrônica de Varredura
LISTA DE SÍMBOLOS
α – alpha β – beta γ – gamma η – eta λ – lambda θ – theta σ – sigma
°C – graus centígrados
μm – micrometro
mm - milimetro
nm - namometro Al – alumínio
Al2O3– óxido de alumínio (alumina)
Ca – cálcio
CaCO3 – carbonato de cálcio
CaHPO4 – monetite
CaHPO4 2(H2O) – brushite
CaO – óxido de cálcio (calcia)
Ca(OH)2 – hidróxido de cálcio
Ca/P – razão cálcio/fósforo
Ca3(PO4)2 – fosfato tricálcio
Ca10(PO4)6(OH)2 – hidroxiapatita estequimétrica
F – flúor h – hora
HPO42- – grupamento hidrogeno fosfato
H3PO4– ácido fosfórico
K – potássio Mg – Magnésio
min - minuto Na – sódio
NH4 - amoníaco
OH- – grupamento hidroxila P – fósforo
pH – potencial hidrogeniônico
PO43- – grupamento fosfato
P2O5– pentóxido de fósforo
rpm – rotação por minuto
SiO2 – óxido de silício (sílica)
TiO2 – dióxido de titânio (titânia)
ZrO2 – dióxido de zircônio (zicônia)
SUMÁRIO
RESUMO ... 10
INTRODUÇÃO ... 20
Objetivo Geral ... 22
Objetivos Específicos ... 23
1 REVISÃO BIBLIOGRÁFICA ... 24
1.1 Introdução aos Biomateriais ... 24
1.2 Biocerâmicas ... 26
1.3 Biocerâmicas de Fosfatos de Cálcio ... 28
1.4 Hidroxiapatita ... 32
1.5 Biomateriais Nanocompósitos à Matriz Hidroxiapatita ... 34
1.6 Nanocompósitos HA/Al2O3-α ... 36
1.7 Compactação ... 40
1.8 Sinterabilidade de Biomateriais ... 41
1.9 Mecânica Linear à Fratura ... 43
1.10 Modos de Fratura das Biocerâmicas ... 46
1.11 Conclusões... 48
2 MATERIAIS E MÉTODOS ... 50
2.1 Carbonato de Cálcio ... 50
2.2 Ácido Fosfórico ... 50
2.3 Síntese do Fosfato de cálcio hidratado e obtenção da Matriz Hidroxiapatita Nanoestruturada ... 51
Fonte: produção do próprio autor. ... 54
2.5 Elaboração dos Pós Nanoestruturados ... 55
2.6 Compactação e Sinterização ... 56
2.7 Preparação dos Corpos de Prova para os Ensaios Mecânicos ... 56
2.8 Caracterização Morfológica e Microestrutural ... 57
2.9 Caracterização Física por Difratometria de Raios X (DRX) ... 57
2.10 Caracterização Química por Espectroscopia de Infravermelho por Transformada de Fourier (FTIR) ... 57
2.11 Análise do Tamanho de Partículas ... 58
2.12 Area Superficial ... 58
2.13 Análise Térmica Diferencial (ATD) e Termogravimetria (TG) ... 59
2.14 Porosidade Aberta e Densidade Hidrostática ... 60
2.15 Resistência de Ruptura à Flexão 3 Pontos ... 61
2.16 Tenacidade à Fratura ... 62
2.17 Relação Entre Tensão de ruptura e Tenacidade à Fratura – Tamanho do Defeito Crítico Teórico ... 64
3 RESULTADOS E DISCUSSÃO ... 66
3.1 Introdução ... 66
3.2 Caracterização das Matérias Primas... 67
3.3 Síntese e Monitoramento do pH ... 78
3.6 Caracterização Química por Espectroscopia de
Infravermelho por Transformada de Fourier (FTIR) ... 95
3.7 Análise do Tamanho de Partícula por Difração à Laser ... 102
3.8 Cálculo Teórico da Área Superficial ... 104
3.9 Análise Térmica Diferencial (ATD) e Termogravimetria (TG) ... 107
3.10 Porosidade Aberta e Densidade Hidrostática ... 108
3.11 Resistência de Ruptura à Flexão Três Pontos ... 111
3.12 Tenacidade à Fratura ... 113
3.13 Relação da Tensão de Ruptura (σR) e Tenacidade à Fratura (KIC) – Tamanho do Defeito Crítico (ac) ... 116
4 CONCLUSÕES ... 123
INTRODUÇÃO
A nanotecnologia abriu novas perspectivas para a qualidade de vida da humanidade em razão dos novos métodos e técnicas utilizados para avaliação, diagnóstico e tratamentos de doenças. Tem contribuído também para o desenvolvimento e elaboração de novos biomateriais com características diferenciadas em relação aos convencionais. Constituídos com novas características microestruturais, nanoestruturais, área superficial de grãos e de microporos, favoráveis à molhabilidade, capilaridade, à adesão e proliferação celular na superfície de grãos e de microporos, promovendo, assim, a melhoria da qualidade interfacial biomaterial/tecido adjacente.
Os biomateriais tem se destacado nas pesquisas por se apresentarem promissores na manutenção do bom funcionamento do organismo. As biocerâmicas nanoestruturadas à base de fosfato de cálcio 𝐶𝑎 𝑃 são uma nova classe de biomateriais que oferecem características diferenciadas em relação aos biomateriais convencionais como bioatividade, área superficial de grãos e de microporos, também apresentam semelhança cristalográfica com a da apatita óssea do esqueleto humano e biocompatibilidade. Estas biocerâmicas podem se dividir em diferentes politipos, assim, diversas composições de fosfatos de cálcio são sintetizadas em diferentes razões molares 𝐶𝑎 𝑃. As composições mais pesquisadas são a hidroxiapatita estequiométrica e o fosfato de cálcio-β, isto devido às características física, química e de solubilidade destas composições, e por serem semelhante à apatita óssea do esqueleto humano. Estas composições já são de uso prático clínico como matrizes sintéticas de reparação de defeitos e reconstituição do tecido ósseo, tanto na medicina como na odontologia, devido sua boa bioatividade e pela capacidade que estes biomateriais apresentam de uma troca iônica em meios biológicos.
Vários métodos de síntese vêm sendo desenvolvidos com o propósito de se obter hidroxiapatita com tamanhos de grãos nanométricos e microestrutura microporosa interconectada. Estas características podem oferecer melhores condições de molhabilidade, capilaridade, adesão celular na superfície de grãos e de microporos, bem como para o interior do biomaterial, assim, favorecendo a osseoindução a osseointegração e a formação do novo tecido ósseo.
nanocompósitos. Os biomateriais compostos de misturas cerâmica/cerâmica são uma prática usual na elaboração de biomateriais nanocompósitos. O interesse na elaboração de biomateriais nanocompósitos está associado às propriedades mecânicas, modificação de morfologia, da arquitetura microestrutural, da área superficial de grãos e de microporos, estas modificações podem contribuir com o gradiente de solubilidade de 𝐶𝑎2+ e 𝑃𝑂
43− para o meio biológico. Outro ponto que deve ser levado em consideração é a microestrutura microporosa interconectada, isto permitirá melhorar a capacidade de molhabilidade e capilaridade do biomaterial.
A elaboração de pós nanocompósitos à matriz hidroxiapatita vem sendo uma prática usual no desenvolvimento de novos biomateriais nanoestruturados. Observa-se na bibliografia um volume crescente de trabalhos que envolvem a elaboração desses biomaterias com a utilização de uma segunda fase nanométrica do tipo 𝐴𝑙2𝑂3− 𝛼, 𝑆𝑖𝑂2, 𝑇𝑖𝑂2𝑛 e 𝑍𝑟𝑂2. Esta segunda fase quando incorporada numa matriz cerâmica de hidroxiapatita, em posição inter-intragranular, pode conduzir a obtenção de biomateriais nanocompósitos com características diferenciadas de propriedades mecânicas, da microestrutura, nanoestrutura e de microporosidade em relação aos biomateriais convencionais.
A 𝐴𝑙2𝑂3− 𝛼 já desempenha importante papel como biomaterial sendo amplamente utilizada em próteses de articulações, em razão deste biomaterial apresentar boas propriedades tribológicas, estabilidade química e resistência à corrosão. Sob a forma de nanopartículas dispersas em posição inter-intragranular dentro de uma matriz hidroxiapatita, pode fornecer um biomaterial nanocompósito com novas características de bioatividade, capilaridade, molhabilidade, microporosidade, área superficial de grãos e de microporos, características favoráveis à viabilidade celular e à reconstituição óssea.
O objetivo deste trabalho se concentrou na síntese de uma matriz hidroxiapatita, elaboração e caracterização de nanocompósitos
𝐻𝐴 𝐴𝑙2𝑂3− 𝛼 sol-gel nanocristalina nas concentrações de 1, 2, 3 e 5%
A elaboração dos pós nanocompósitos foi realizada com ajuda de um moinho atritor de alta energia, álcool etílico e esferas de zircônia. Esse processo foi utilizado com objetivo de obter uma melhor dispersão da segunda fase alumina-α nanométrica na matriz hidroxiapatita. Foram elaboradas cinco composições de pós nanoestruturados: o pó nanoestruturado de hidroxiapatita (matriz óssea), depois os pós nanocompósitos com 1%, 2%, 3% e 5%, em volume de 𝐴𝑙2𝑂3− 𝛼. Os resultados apresentados estão relacionados ao método de síntese, via úmida, à elaboração e caracterização dos pós nanoestruturados de hidroxiapatita e nanocompósitos 𝐻𝐴 𝐴𝑙2𝑂3− 𝛼, e corpos de prova. Os estudos de caracterização foram realizados utilizando as seguintes técnicas: Microscopia Eletrônica de Varredura para observação da morfologia dos pós nanoestruturados e superfície de fratura dos corpos de prova recuperados do ensaio meânico; Difratometria de Raios X para a identificação das fases cristalinas; Análise Térmica Diferencial para se avaliar as mudanças de fases no processo de elaboração da alumina-α e da fase hidroxiapatita; Espectrometria de Infravermelho por Transformada de Fourier para avaliação das bandas vibracionais dos grupamentos 𝑂𝐻− e 𝑃𝑂
43−, além de estudos de porosidade, densidade e análise da distribuição do tamanho de partículas. Para determinação das propriedades mecânicas, os ensaios foram realizados em flexão à três pontos, onde se determinou a tensão de ruptura e o coeficiente de tenacidade à fratura.
Objetivo Geral
Este trabalho teve como objetivo sintetizar uma matriz hidroxiapatita nanoestruturada pelo método de síntese via úmida e elaborar biomateriais nanoestruturados 𝐻𝐴 𝐴𝑙2𝑂3− 𝛼 sol-gel nanométrica, nas concentrações 1%, 2% 3% e 5% em volume.
Objetivos Específicos
Sintetizar a matriz hidroxiapatita através do processo via úmido.
Sintetizar as nanopartículas de alumina-, utilizadas como segunda fase, pelo processo sol gel.
Elaborar pós nanocompósitos 𝐻𝐴 𝐴𝑙2𝑂3− 𝛼 sol-gel utilizando o método por moinho atritor de alta energia.
Sinterizar pós nanoestruturados de hidroxiapatita e nanocompósitos 𝐻𝐴 𝐴𝑙2𝑂3− 𝛼 para obtenção de biomateriais nanoestruturados.
1 REVISÃO BIBLIOGRÁFICA
1.1 Introdução aos Biomateriais
A evolução dos biomateriais está associada às necessidades e a procura da humanidade por uma melhor qualidade de vida. Os acontecimentos naturais e catastróficos, resultantes de diferentes fenômenos ocorridos no planeta, gerados pelo homem ou pelo próprio sistema natural, tem conduzido ao desenvolvimento de pesquisas em diferentes áreas do conhecimento. A evolução da consciência humana tem proporcionado às ciências físicas, químicas, biológicas e de materiais, obterem melhor compreensão dos fenômenos que envolvem estes meios. Proporcionando, ainda, o desenvolvimento de novos biomateriais capazes de exercer as funções necessárias dentro dos processos cirúrgicos, o que tem proporcionado uma melhoria da qualidade de vida e longevidade dos seres humanos [BOSE, 2002, VALLET-REGÍ, 2001].
O período da Segunda Guerra Mundial foi um marco importante para as pesquisas e desenvolvimento de biomateriais. Isto se justifica pelo volume de militantes mutilados pós-guerra, gerando preocupações governamentais e da humanidade. Por essa razão passou a existir grande interesse governamental e por diferentes laboratórios de pesquisa em desenvolver biomateriais e dispositivos que pudessem substituir membros ou partes de membros tidos como não funcionais, que fossem capazes de oferecer melhor conforto e qualidade de vida, principalmente aos combatentes mutilados [KARVAT, 2005]. Neste período se deu maior ênfase aos biomateriais metálicos pela facilidade de elaboração de próteses e materiais de substituição do esqueleto.
biomateriais se destacam os metálicos de titânio, ligas de titânio, alguns biomateriais poliméricos e as biocerâmicas [GEMELLI, 2012; KAVACHI, 2000]. A tabela 1 apresenta diferentes tipos de biomateriais e suas aplicações biomédicas.
Tabela 1 - Relação entre alguns biomateriais sintéticos e suas aplicações.
Biomaterial Aplicações
Polímeros Suturas, artérias, veias; maxilofacial
(nariz, orelha), tendão artificial, oftalmologia.
Polietileno, poliéster, poliuretano
Metais e ligas
Fixação ortopédica (parafusos, pinos), implantes dentários.
Aço inoxidável, liga de titânio, liga de cobalto-cromo
Cerâmicas e vidros
Ossos, dentes, válvulas, tendões, traquéias artificiais.
Alumina, zircônia, fosfatos de cálcio, vidros bioativos
Fonte: Adaptado de KAVACHI, 2000.
Os novos métodos e técnicas de síntese e de elaboração de biomateriais tem levado ao desenvolvimento de pós micro e nanoestruturados e de biomateriais capazes de oferecer melhores características de bioatividade, biocompatibilidade e de biofuncionalidade. A engenharia de tecidos tem contribuído na avaliação do comportamento destes biomateriais em estudos in vitro e in vivo, fornecendo resultados sobre o comportamento da viabilidade celular, da citotoxicidade, da adesão e proliferação celular na superfície e para o interior do biomaterial [LIU, 2008].
Os biomateriais nanoestruturados absorvíveis ou biodegradáveis são uma nova classe de biomateriais, desenvolvidos com interesse de atuação na reparação de defeitos e na formação tecidual. Esta nova classe de biomateriais tem se apresentado favorável em aplicações biomédicas, por oferecerem condições de reparação tecidual e de formação de um novo tecido de forma diferenciada dos biomateriais convencionais.
1.2 Biocerâmicas
Constatou-se na bibliografia que, no decorrer das últimas décadas, houve uma evolução significativa das pesquisas sobre biomateriais de reparo e reconstrução tecidual para aplicações biomédicas. Esta evolução está associada às necessidades da humanidade e aos interesses comerciais e governamentais em oferecer melhor qualidade de vida à população. A partir da década de 60 houve grandes esforços realizados por diferentes laboratórios de pesquisa, sobre o desenvolvimento de biocerâmicas microestruturadas para uso como biomaterial de implante e/ou como matriz óssea, na reparação de defeitos ósseos [BEST, 2008, BOSE, 2002]. A partir da década de 90, observou-se um volume crescente de novas biocerâmicas para uso como biomaterial de implante, de reparação e reconstituição óssea. Dentre estas biocerâmicas, se destacam as biocerâmicas de alumina-, zircônia, os biovidros e as biocerâmicas de fosfatos de cálcio.
classe de biomateriais que vem sendo pesquisada e desenvolvida por diferentes centros de pesquisa. O interesse se encontra em obter biomateriais com características diferenciadas dos biomateriais convencionais autógenos, alógenos e exógenos. Esta nova classe de biomateriais cerâmicos é composta pelas biocerâmicas bifásicas e os biomateriais nanocompósitos à matriz cerâmica de hidroxiapatita e/ou fosfato de cálcio-. Essas biocerâmicas vêm se apresentando promissoras em aplicações biomédicas, o que poderá num futuro próximo, serem capazes de substituir efetivamente os biomateriais convencionais de reparação e de reconstituição óssea [CAMARGO, 2012, BOSE, 2002, GAUTIER, 1999].
A síntese e elaboração de biocerâmicas nanoestruturadas têm despertado interesses científicos, de mercado, políticos, governamentais e sociais [OLIVEIRA, 2010; CAMARGO, 2009 (b)]. Isto se deve em razão desta nova classe de biomateriais apresentar características diferenciadas de área superficial de grãos e de microestruturas com microporos interconectados. Apresentam ainda melhores características de solubilidade em razão das novas propriedades superficiais da morfologia de grãos e da microporosidade interconectada, o que pode controlar a solubilidade destes, quando aplicadas em meios biológicos
[CAMARGO, 2012, DALMÔNICO 2011, CAMARGO 2009 (a), WEBSTER 2000].
As biocerâmicas nanoestruturadas de fosfato de cálcio, são materiais sólidos, inorgânicos e quimicamente inertes [GILAPA 2001].
São constituídos, de uma maneira geral, por uma ou mais fases descontínuas dispersas dentro de uma fase contínua, sendo a fase descontínua da ordem nanométrica 𝑑< 100 𝑛𝑚 . Para o caso da fase descontínua de natureza diferente dispersa dentro da fase contínua, o material nanoestruturado é chamado de híbrido ou nanocompósito [BELLINI, 2007, SILVA 2007].
Existe uma grande expectativa nesta nova classe de biomateriais. Pesquisas realizadas por diferentes autores
contribuindo de maneira progressiva dentro dos processos de neoformação e reconstrução óssea [WEBSTER, 1999].
As biocerâmicas nanoestruturadas são uma nova classe de biomateriais que vem se apresentando promissoras em aplicações biomédicas na reparação de defeitos ósseos. Estudos realizados recentemente in vivo[CANULLO 2009], demonstraram que os fosfatos de cálcio nanoestruturados sintéticos, com microporosidade e microestruturas controladas, podem gerar resultados diferenciados e mesmo superiores de neoformação óssea, em relação aos biomateriais convencionais.
1.3 Biocerâmicas de Fosfatos de Cálcio
Existem diferentes polítipos de fosfatos de cálcio que juntos formam uma família de compostos conhecidos por „apatitas‟. Esses compostos representam uma das famílias de biomateriais mais complexas devido a grande variedade nas composições 𝐶𝑎 𝑃
[KUMTA, 2005, RAMAY, 2004]. Os fosfatos de cálcio podem ser obtidos por diferentes métodos e técnicas de síntese. Os politipos mais conhecidos e pesquisados atualmente são: o fosfato tricálcio 𝑇𝐶𝑃 , na composição química 𝐶𝑎3 𝑃𝑂4 2 e a hidroxiapatita na composição química 𝐶𝑎10 𝑃𝑂4 6 𝑂𝐻 2. Estes biomateriais se destacam nas pesquisas por serem compostos inorgânicos semelhantes à estrutura da fase mineral do osso, dentina e esmalte dentário [CAMARGO, 2009 (a)].
O fosfato de cálcio existe sob duas formas polimórficas, sendo que a baixas temperaturas encontra-se na forma alotrópica TCP- e a altas temperaturas, acima de 1180oC, na fase 𝑇𝐶𝑃 − 𝛼[BELLINI, 2007; ELLIOTT, 1994].
Estudos realizados por diferentes autores sobre o comportamento da solubilidade dos fosfatos de cálcio têm demonstrado resultados diferenciados entre as composições. Observou-se que a dissolução do 𝑇𝐶𝑃 − 𝛽 é de 3-12 vezes mais rápida que a da hidroxiapatita estequiométrica 𝐶𝑎10 𝑃𝑂4 6 𝑂𝐻 2,𝐻𝐴 , constatou-se também que o 𝑇𝐶𝑃 − 𝛼 apresentou, uma taxa de dissolução superior ao
𝑇𝐶𝑃 − 𝛽. A ordem de solubilidade relativa do 𝑇𝐶𝑃 − 𝛼, 𝑇𝐶𝑃 − 𝛽 e 𝐻𝐴
solubilidade superior, faz destes biomateriais promissores em aplicações de reparo e de reconstituição óssea quando implantados num meio biológico, sendo absorvíveis gradualmente formando uma nova estrutura óssea [LIN, 2001.
O processo de solubilidade das biocerâmicas de fosfatos de cálcio por organismos vivos ocorre por dois mecanismos:
a) o primeiro trata-se da dissolução natural do material em meio fisiológico devido à troca cátion/iônica dos íons cálcio e fósforo;
b) o segundo refere-se ao processo de fagocitose celular. Freqüentemente, os produtos da degradação são observados nos fagócitos, célula que realiza fagocitose, em regiões intra e extracelulares, próximas ao material biocerâmico injetado ou implantado. O tamanho, forma e a topografia de superfície das partículas e/ou de grãos de fosfatos de cálcio podem favorecer, ou não, a solubilidade do biomaterial e formação de um tecido ósseo precoce, isto se deve às características das partículas e da microporosidade existente entre elas [OOMS, 2003].
Estes fosfatos de cálcio podem apresentar capacidade de hidratação quando na forma de biocimentos que, em presença de solução líquida, decompõe-se em diferentes politipos cristalinos ou amorfos dentro da massa de biocimento. Os biocimentos podem ainda ser conformados e/ou moldados na forma deseja, assim possibilitando aplicação e/ou preenchimento completo de cavidades. Mas é importante lembrar, que os biomateriais de fosfato de cálcio, de maneira geral, apresentam baixas propriedades mecânicas, no máximo chegando a valores semelhantes ao do osso cortical ou trabecular. Isto tem limitado a utilização destes biomateriais em aplicações biomédicas sujeitas a solicitações mecânicas severas [BELLINI, 2007].
alógenos, exógenos e, até mesmo, os autógenos [TADIC, 2004, YUAN, 1999].
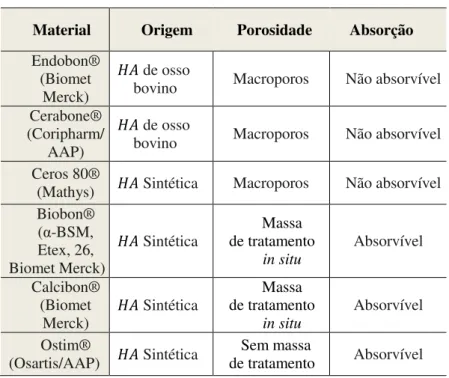
Atualmente há diferentes marcas comerciais de substitutos ósseos à base de fosfato de cálcio disponíveis no mercado. A tabela 2 apresenta diferentes biomateriais com suas características de microporosidade e de adsorção em meios biológicos.
Tabela 2 - Origem e composição de substitutos ósseos inorgânicos
Material Origem Porosidade Absorção
Endobon® (Biomet
Merck)
𝐻𝐴 de osso
bovino Macroporos Não absorvível
Cerabone® (Coripharm/
AAP)
𝐻𝐴 de osso
bovino Macroporos Não absorvível
Ceros 80®
(Mathys) 𝐻𝐴 Sintética Macroporos Não absorvível
Biobon® (α-BSM, Etex, 26, Biomet Merck)
𝐻𝐴 Sintética
Massa de tratamento insitu Absorvível Calcibon® (Biomet
Merck) 𝐻𝐴 Sintética
Massa de tratamento
in situ
Absorvível
Ostim®
(Osartis/AAP) 𝐻𝐴 Sintética Sem massa de tratamento Absorvível
Fonte: Adaptado de SCHNETTLER, 2004.
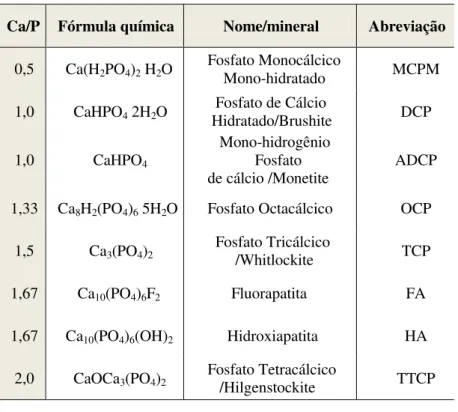
Tabela 3 - Razão molar, Fórmula e nome químico de algumas composições de fosfatos de cálcio.
Ca/P Fórmula química Nome/mineral Abreviação
0,5 Ca(H2PO4)2 H2O Fosfato Monocálcico Mono-hidratado MCPM
1,0 CaHPO4 2H2O Fosfato de Cálcio Hidratado/Brushite DCP
1,0 CaHPO4
Mono-hidrogênio Fosfato
de cálcio /Monetite ADCP 1,33 Ca8H2(PO4)6 5H2O Fosfato Octacálcico OCP
1,5 Ca3(PO4)2 Fosfato Tricálcico /Whitlockite TCP
1,67 Ca10(PO4)6F2 Fluorapatita FA
1,67 Ca10(PO4)6(OH)2 Hidroxiapatita HA
2,0 CaOCa3(PO4)2 Fosfato Tetracálcico /Hilgenstockite TTCP
Fonte: GROOT, 1998.
1.4 Hidroxiapatita
A hidroxiapatita de formula química 𝐶𝑎10 𝑃𝑂4 6 𝑂𝐻 2, tem composição de 39,68% em peso de cálcio e 18,45% em peso de fósforo, resultando em uma razão 𝐶𝑎 𝑃 de 1,667 molar [BEST, 2008]. Apresenta estrutura cristalina hexagonal compacta cujos parâmetros de rede são 𝑎=𝑏= 0,942 𝑛𝑚 e 𝑐= 0,687 𝑛𝑚, com plano principal de difração [211] [JCPDS corresponde à ficha 74-0565]. Sua célula unitária é formada pelos íons 𝐶𝑎2+, 𝑃𝑂
43− e 𝑂𝐻−, onde o arranjo hexagonal é construído pelos íons 𝐶𝑎2+ e 𝑃𝑂
43− sobre colunas de 𝑂𝐻−
[DOURADO, 2006]. A figura 1 apresenta um esquema da malha unitária da estrutura cristalina da hidroxiapatita ao longo do eixo “c”, onde uma das colunas de 𝑂𝐻− é ilustrada [ELLIOTT, 1994].
Figura 1 - Representação da malha unitária da estrutura cristalina da hidroxiapatita ao longo do eixo “c”.
As apatitas biológicas diferem da sintética por possuírem outros elementos em sua estrutura. Íons como 𝑀𝑔2+, 𝑁𝑎+ e 𝐾+ podem ser encontrados em sua estrutura ao substituírem um ou mais 𝐶𝑎2+[CHOI,
2006]. Dessa forma as apatitas biológicas são sempre deficientes em cálcio por serem capazes de trocar seus íons por outros elementos. Essa capacidade de fazer substituições lhes confere uma de suas maiores propriedades ao atuar como um reservatório de cálcio e fósforo e como um sistema regulador de diferentes íons nos fluidos corporais
[DALMÔNICO, 2011]. Essas substituições alteram os parâmetros da rede cristalina da hidroxiapatita, podendo alterar sua cristalinidade e as propriedades de solubilidade e mecânicas do biomaterial. Observou-se na bibliografia que, de maneira geral, as hidroxiapatitas sintéticas apresentam arranjos cristalinos mais bem definidos se comparados com as biológicas [KUMTA, 2005]. A melhor cristalinidade da hidroxiapatita sintética é obtida devido às altas temperaturas empregadas em sua produção.
Atualmente existem diferentes métodos e técnicas utilizados para síntese de pós de hidroxiapatita nanométrica, dentre estes se destacam o método por dissolução/precipitação sólido/líquido, reação hidrotermal e o processo sol-gel. O método baseado na dissolução/precipitação, também chamado de síntese via úmida, consiste basicamente em dissociar os precursores de íons cálcio e fósforo para formação dos fosfatos de cálcio, em meio aquoso. Dentre os métodos utilizados, um que se apresenta vantajoso é o que ocorre pela reação entre o 𝐶𝑎 𝑂𝐻 2 e 𝐻3𝑃𝑂4 em meio aquoso. Isso devido apresentar baixo custo para obtenção dos fosfatos de cálcio associada à simplicidade do método, além de deixar a água como o único material remanescente.
A síntese por reação hidrotermal promove a formação de precipitados de fosfatos de cálcio a partir de soluções aquosas a temperaturas relativamente elevadas, em torno de 140 à 500°C, para formação da fase hidroxiapatita. O processo também necessita de elevadas pressões para que o solvente não volatize. Alguns fosfatos de cálcio são usados como precursores para a síntese de hidroxiapatita por esse método, como a monetite 𝐶𝑎𝐻𝑃𝑂4 e a brushite
𝐶𝑎𝐻𝑃𝑂4 2 𝐻2𝑂 .
obtendo, normalmente, pós com estruturas amorfas ou semicristalinas nanométricas. Com o posterior tratamento térmico, se obtém a fase hiroxiapatita nanométrica [CAMARGO, 1995].
É sabido que as condições de síntese e processamento influenciam diretamente na razão molar 𝐶𝑎/𝑃 e estequiometria dos fosfatos de cálcio [DOURADO, 2006]. Diferentes razões 𝐶𝑎/𝑃 podem ser sintetizadas dependo do método de síntese adotado e as condições empregadas [KUMTA, 2005, BEST, 2008]. Dentre os diferentes polítipos de fosfatos de cálcio, a hidroxiapatita estequiométrica
𝐶𝑎 𝑃= 1,67 molar , por apresentar similaridade cristalográfica com
a fase mineral dos ossos, pela sua boa bioatividade e biocompatíbilidade, se destaca como biomaterial de reparação de tecidos duros [SAHOO, 2013, CHOI, 2006].
1.5 Biomateriais Nanocompósitos à Matriz Hidroxiapatita
Os nanocompósitos biocerâmicos são materiais sólidos, inorgânicos, constituídos de uma maneira geral de uma ou muitas fases descontínuas dispersas dentro de uma fase contínua, sendo a fase descontínua de ordem nanométrica 𝑑< 100 𝑛𝑚 .
A adição de uma segunda fase descontínua na forma de nanopartículas, fibras ou plaquetas dentro de uma fase contínua denominada de matriz cerâmica, pode ter como interesse duas possibilidades:
a) Modificar as características da microestrutura, da nanoestrutura e da superfície de grãos e microporos, procurando melhorar a solubilidade, a adesão e proliferação celular na superfície de grãos e de microporos dos nanomateriais.
b) Melhorar as propriedades mecânicas, principalmente minimizar o problema da fratura frágil, assim, procurando melhorar o valor do coeficiente de tenacidade à fratura da matriz cerâmica.
Figura 2 - Esquema representativo da distribuição da segunda fase na matriz cerâmica [NIHARA, 1999].
Fonte: NIHARA, 1999.
de hidroxiapatita, pode também influenciar sensivelmente o processo de dispersão da segunda fase na matriz hidroxiapatita, o que poderá levar à formação de agregados em contornos de grãos, inibindo a sinterabilidade e conduzindo a certo número de defeitos na microestrutura do biomaterial [BELLINI, 2007, KARVAT, 2005].
Os biomateriais nanocompósitos à matriz hidroxiapatita/ Al2𝑂3− 𝛼, 𝑆𝑖𝑂2𝑛, 𝑍𝑟𝑂2𝑛 e 𝑇𝑖𝑂2𝑛, a segunda fase pode conduzir a presença de tensões residuais termoelásticas, ocasionadas pela diferença dos coeficientes de dilatação das fases, geradas durante o processo de sinterização e do resfriamento do biomaterial, podendo levar ao surgimento de micro trincas, ou mesmo à degradação total do biomaterial [BELLINI, 2007, BARRALET, 2000].
1.6 Nanocompósitos HA/Al2O3-α
Os biomateriais nanocompósitos de hidroxiapatita/Al2𝑂3− 𝛼, vem sendo desenvolvidos e pesquisados sob dois pontos:
1º elaborar biomateriais nanocompósitos com novas características de propriedades mecânicas, o que nem sempre é possível, quando se utiliza uma matriz cerâmica de hidroxiapatita [SOUZA, 2009, DELIMA, 2009, KARVAT, 2005].
2º desenvolver novos biomateriais com microporosidade interconectada, grãos mais finos, área superficial de grãos e de microporos elevada, o que pode melhorar sensivelmente a capilaridade, a molhabilidade, fornecendo melhores condições à adesão e proliferação celular na superfície de grãos e de microporos, contribuindo com os processos de reparação e reconstrução óssea [CAMARGO, 2012, SANTOS, 2009, BELLINI, 2007].
a osseoindução e adesão do tecido ósseo na interface do biomaterial
[JUN, 2003, KIM, 2002].
A utilização de nanopartículas de alumina- vem sendo uma prática utilizada na elaboração de biomateriais nanocompósitos. Quando utilizada como segunda fase dispersa dentro de uma matriz cerâmica de hidroxiapatita, esta pode se desestabilizar durante o processo de sinterização do nanomaterial, em razão da temperatura, onde pode ocorrer a transformação da fase de fosfato de cálcio- e/ou a em aproximadamente 1180ºC. Durante o processo de sinterização pode ocorrer a liberação de 𝐶𝑎𝑂 pela desestabilização da fase hidroxiapatita, o que pode conduzir a formação de aluminatos de cálcio. Sabe-se da bibliografia que a formação das fases de aluminatos de cálcio também está associada à quantidade em volume da segunda fase utilizada na elaboração do nanomaterial [KARVAT, 2005]. As modificações de fases no estado sólido em biomateriais nanocompósitos cerâmicos, cujas ligações são predominantemente iônicas, ocorrem pela difusão dos íons através da interface nos contornos de grãos [VISWANATH, 2006]. Para os nanocompósitos 𝐻𝐴 𝐴𝑙2𝑂3− 𝛼, os íons responsáveis pela formação de aluminatos de cálcio são o 𝐶𝑎2+ e o 𝐴𝑙3+. A difusão dos íons 𝐴𝑙3+ ocorre na interface dos grãos da alumina- e a difusão dos íons 𝐶𝑎2+ são provenientes do CaO resultantes da decomposição da fase 𝐻𝐴 em 𝑇𝐶𝑃 − 𝛽 [VISWANATH, 2006, EVIS , 2007, JUN, 2003]. Estas transformações de fase ocorrem a altas temperaturas através da difusão interfacial de grãos entre a matriz e segunda fase alumina-, conduzindo a transformação de aluminatos de cálcio
[VISWANATH, 2006]. Portanto, a presença de uma pequena concentração de alumina- nanométrica na matriz hidroxiapatita pode alterar a cinética de difusão superficial da hidroxiapatita favorecendo sua decomposição em 𝑇𝐶𝑃 − 𝛽 ou e formação das fases de aluminatos de cálcio[CAMARGO, 2009 (b), JUN, 2003].
De acordo com o diagrama de fase 𝐶𝑎𝑂 − 𝐴𝑙2𝑂3 (Fig. 3), o 𝐶𝑎2+ é a espécie que difunde na Al
2O3. Normalmente parte da
hidroxiapatita estequiométrica se decompõe em 𝑇𝐶𝑃 − 𝛽 em torno de 1180°C [DALMÔNICO, 2011], e a temperatura de 1400°C, conduz a decomposição da fase hidroxiapatita estequiométrica e do fosfato de cálcio- em 𝑇𝐶𝑃 − 𝛼. Porém, para os biomateriais nanocompósitos de
𝐻𝐴 𝐴𝑙2𝑂3− 𝛼a presença da segunda fase alumina-nanométrica em
[VISWANATH, 2006]. Observou-se na bibliografia, para o caso dos biomateriais nanocompósitos 𝐻𝐴 𝐴𝑙2𝑂3− 𝛼nanométrica, que a segunda fase nanométrica influencia fortemente no processo de decomposição da fase 𝐻𝐴 em 𝑇𝐶𝑃 e 𝐶𝑎𝑂, o que desestabiliza a fase alumina-, conduzindo a formação de aluminatos de cálcio [SOUZA, 2009, VISWANATH, 2006, EVIS, 2007]. A figura 4 ilustra o mecanismo como ocorre o processo de difusão interfacial entre
𝐻𝐴 𝐴𝑙2𝑂3− 𝛼, mostrando a difusão do 𝐶𝑎2+ proveniente da
hidroxiapatita, o que leva a modificação da razão Ca/P da hidroxiapatita através da difusão interfacial desses íons, conduzindo a transformação das fases de fosfato de cálcio- e/ou e aluminatos de cálcio
[VISWANATH, 2006, EVIS, 2007].
Figura 3 - Diagrama de fases 𝐶𝑎𝑂 − 𝐴𝑙2𝑂3.
Figura 4 - Esquema representativo do processo de difusão interfacial
𝐻𝐴 𝐴𝑙2𝑂3− 𝛼.
Fonte: VISWANATH, 2006. Nota: AL refere-se aos aluminatos de cálcio.
Estas transformações podem ocorrer a temperaturas relativamente baixas em razão da presença da segunda fase nanométrica em posição inter-intragranular na matriz hidroxiapatita, o que pode favorecer a desestabilização das fases a temperaturas mais baixas, conforme pode ser observado na figura 3 [VISWANATH, 2006].
de sua adsorção pelo meio biológico ou simulado [OLIVEIRA, 2010, BEST, 2008, TANCRED, 1998]. Esta nova classe de biocerâmicas bifásicas e/ou nanocompósitos vem sendo desenvolvidos na forma de biomateriais granulados, que pelo processo de sinterização fornecem grânulos com microestruturas microporosas interconectadas, apresentando boas características de molhabilidade, capilaridade, sendo favoráveis à adesão celular nos contornos dos biomateriais granulados, bem como nos contornos de grãos, na superfície de microporos e para o interior do biomaterial granulado microporoso, assim, dando melhores condições aos processos de reparo e reconstrução óssea [DALMÔNICO, 2011, CAMARGO, 2009 (b), LEGEROS, 2008, CAMARGO, 2007, TADIC, 2004, JUN, 2003].
1.7 Compactação
A compactação é um método utilizado para conformação de pós biocerâmicos e/ou pós metálicos obtidos pela metalurgia do pó. Este método consolida o pó solto na forma desejada através da aplicação de uma carga mecânica. Na indústria o método de conformação mais utilizado é a compactação uniaxial por possibilitar a fabricação rápida de peças com precisão dimensional e relativa complexidade de forma.
Figura 5 - Diagrama de compactação dos pós biocerâmicos.
Fonte: JORAND, 1991.
1.8 Sinterabilidade de Biomateriais
A sinterabilidade de pós biocerâmicos é uma parte importante dentro dos processos de elaboração de biomateriais. Durante o processo de sinterização pode ocorrer mudanças superficiais e transformações de fases simultaneamente ou consecutivamente. A sinterização é um processo normalmente realizado após a compactação do pó que poderá ser submetido a um
Ruptura dos aglomerados
Ruptura e deformação elástica
Ruptura dos agregados mais finos
𝑃 (𝑀𝑃𝑎) 𝑃𝑦
tratamento térmico e após, a sinterização. A temperatura escolhida para sinterização deve ser inferior à de fusão do constituinte principal do pó biocerâmico que constituirá o biomaterial final, geralmente de 1/2 a 2/3 da sua temperatura de fusão, assim formando um sólido coerente único. O biomaterial recuperado da sinterização poderá apresentar propriedades ótimas ou não.
O processo de sinterização ocorre através da redução da energia livre da superfície do compactado pela ligação das interfaces das partículas vizinhas, promovendo a modificação das interfaces gás/solido para interfaces sólido/sólido de energia livre inferior. Posteriormente ocorre a coalescência dos grãos, empescoçamento, o que conduz a redução entre os contornos de grãos e redução da porosidade aberta, levando à densificação do biomaterial
[CAMARGO, 2009 (b)]. A figura 6 mostra as etapas do processo de sinterização de biocerâmicas relacionando as interfaces: gás/sólido (a), sólido/sólido (b), coalescência dos grãos, fechamento da porosidade e contornos de grãos (c).
Figura 6 - Esquema representativo da sinterização de pós compactados: (a) pó inicial, (b) coalescência de grãos, (c) Interface de grãos e fechamento da porosidade.
Fonte: CALLISTER JR, 2002.
composição do material e atmosfera de sinterização. Em se tratando de uma matriz hidroxiapatita, a temperatura empregada na sinterização pode afetar negativamente sua resistência. Isso acontece, pois, quando exposta à temperaturas relativamente elevadas a hidroxiapatita tende a eliminar o grupo funcional OH-, podendo resultar em sua decomposição nas fases 𝑇𝐶𝑃 − 𝛽 e
𝑇𝐶𝑃 − 𝛼. Esse processo inibe a densificação, comprometendo as
propriedades mecânicas [MURALITHRAN, 2000, TAMPIERI, 2000]. Em se tratando de compósitos 𝐻𝐴 𝐴𝑙2𝑂3− 𝛼, a quantidade em volume de alumina-α dentro da matriz hidroxiapatita em posição inter-intragranular, juntamente com a temperatura de sinterização, podem levar à modificação das interfaces através do processo de difusão interfacial das fases, conduzindo uma degradação da fase hidroxiapatita levando à transformação de fases de aluminados de cálcio[VISWANATH, 2006].
1.9Mecânica Linear à Fratura
A mecânica da fratura baseia-se na teoria de Grifttih que estabelece uma relação entre a concentração de tensão no defeito com a tensão aplicada no material. Essa teoria pode ser aplicada em estudos do comportamento mecânico de biomateriais cerâmicos, onde se considera estes como sendo sólidos frágeis, contendo defeitos de microporosidade ou micro-trincas pré-existentes da ordem microscópica. A presença destes defeitos pode contribuir com a propagação das micro-fissurações dentro do biomaterial, provocando concentração de tensões localizadas nas interfaces de grãos, podendo inclusive ultrapassar os valores limite de resistência interfacial do biomaterial.
1.9.1 Teoria de Griffith
propagação de uma micro-fissura preexistente com forma elíptica de comprimento
2
𝑎
, dentro de uma placa infinita unitária, solicitada de maneira uniforme (Fig. 7). Para o caso de biomateriais cerâmicos, existe uma liberação de energia de deformação elástica, ou seja, uma parte da energia que é armazenada no biomaterial à medida que ele é submetido a um carregamento dentro da zona de deformação elástica. Além disso, durante o processo de extensão da micro-trinca, são criadas nas faces de uma micro-trinca novas superfícies livres que dão origem ao aumento na energia de superfície do sistema.
Figura 7 - Representação esquemática de uma fissura interior elíptica numa placa infinita de espessura uniforme.
Fonte: produção do próprio autor.
Griffith desenvolveu um critério de propagação de trinca para uma trinca elíptica pela execução de um balanço energético. A energia total do sistema é representada pela equação 1:
𝑈𝑡 = 𝑈𝑒0+ 4∙ 𝑎 ∙ 𝛾𝑠− 𝜋 𝑎
2∙𝜎2
Onde:
𝑈𝑒0 = energia elástica da placa na ausência de fissura
4∙ 𝑎 ∙ 𝛾𝑠 = energia superficial de fissura
𝜋 𝑎2∙𝜎2
𝐸 = termo que corresponde à energia elástica devido à fissura
𝐸
= módulo de elasticidade do material.
A soma das energias passa por um máximo no momento que a falha atinge um valor crítico 𝑎𝑐, e a fissura se propaga de maneira
catastrófica.
A aproximação da resistência à ruptura consiste em calcular as concentrações de tensões induzidas por um defeito dentro de um modelo idêntico. Isto conduz a uma definição do coeficiente de intensidade de tensões 𝐾determinado para um tamanho máximo de um entalhe (raio no fundo do entalhe 𝑟0). O critério 𝐾 é calculado para cada um dos três modos fundamentais de fratura: tração, compressão e torção. A ruptura ocorre quando 𝐾 atinge um valor crítico 𝐾𝐶 que é a
medida em termos de fator de intensidade da tensão de ruptura e em relação a um tamanho crítico de fissura
𝑎
𝑐 de acordo com a equação 2:
𝐾𝐼𝐶 =𝑌 ∙ 𝜎𝑅∙ 𝜋 ∙ 𝑎𝑐 Equação 2
Onde:
𝑌
= parâmetro de forma
𝜎𝑅 = tensão de ruptura𝑎𝑐
= comprimento da trinca
𝐾𝐼𝐶
= fator de intensidade de tensão no modo
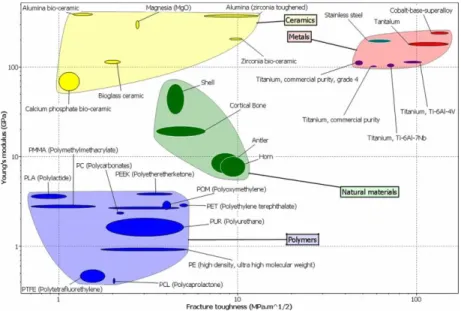
𝐼 (abertura ou tração).compactado estão relacionadas principalmente aos constituintes da biocerâmica, da qualidade de interface e sua densificação. Portanto, os valores de resistência mecânica e tenacidade à fratura estão associados à obtenção de biomateriais sinterizados com densidade hidrostática próxima da densidade teórica. Outra forma de melhorar a densidade e as características de propriedades mecânicas das biocerâmicas é através da incorporação de uma segunda fase, obtendo um biomaterial compósito ou nanocompósito, o que pode conferir novas características, por vezes antagônicas. Para o caso de biomateriais compósitos, constituídos de diferentes fases, a diferença dos coeficientes de dilatação das fases presentes está associada à presença de tensões termoelásticas, geradas durante o processo de transformações de fase, crescimento de grãos e durante o resfriamento do biomaterial, podendo levar ao surgimento de micro trincas, ou mesmo à degradação total do biomaterial [BARRALET, 2000, CAMARGO, 1995]. As propriedades comumente determinadas são o Módulo de Elasticidade 𝐸 , a Resistência à fratura 𝜎𝑅 e o coeficiente de Tenacidade à fratura 𝐾𝐼𝐶 . A figura 8 mostra um comparativo do comportamento do osso cortical com os diversos biocerâmicos monolíticos e compósitos em relação ao Módulo de Elasticidade e Tenacidade à fratura.
1.10 Modos de Fratura das Biocerâmicas
As biocerâmicas micro e nanoestruturadas podem apresentar três modos de fratura: a) intergranular, b) inter-intragranular e c) completamente transgranular.
a) O primeiro ocorre com a propagação da trinca nas interfaces de grãos, que corresponde à quebra sucessiva e repetida das interfaces de grãos;
Figura 8 - Ilustrando as propriedades mecânicas de diferentes biomateriais.
Fonte: BUTSCHER, 2011.
c) O terceiro modo ocorre através do rompimento sucessivo dos planos cristalográficos por clivagem ou cisalhamento conduzindo uma fratura através dos grãos.
1.11 Conclusões
O estudo bibliográfico serviu de apoio para ampliação do conhecimento científico sobre as pesquisas relacionadas aos biomateriais nanoestruturados que vem sendo utilizados como substitutos na reparação e reconstrução do tecido ósseo. Este estudo propiciou melhor compreensão sobre as características das biocerâmicas nanoestruturadas à base de fosfato cálcio e suas aplicações biomédicas. Observou-se uma variedade de composições de fosfatos de cálcio sendo as mais conhecidas em aplicações biomédicas a hidroxiapatita e o fosfato de cálcio-, por apresentarem semelhança química e física com a apatita óssea. Outra constatação foi as diferentes propriedades de solubilidade apresentada por essas composições. Observou-se na bibliografia que os biomateriais de composições bifásicas e nanocompósitos à matriz hidroxiapatita melhoram as características de solubilidade da fase hidroxiapatita. Também se constatou que esse biomateriais se mostram promissores em aplicações biomédicas na reconstituição de tecidos ósseos danificados por apresentarem melhores características de superfície de área e de solubilidade quando aplicados em meios biológicos in vivo ou simulado.
2 MATERIAIS E MÉTODOS
Nesta parte do trabalho serão descritos as matérias-primas e suas características. O método de síntese utilizado para obtenção da matriz cerâmica de hidroxiapatita nanoestruturada, o método sol-gel para obtenção da alumina-α sol-gel e a metodologia utilizada para elaboração dos pós nanocompósitos e obtenção dos corpos de prova. Também serão apresentados a seguir, os métodos e técnicas utilizados para caracterização das diferentes composições dos pós nanoestruturados e de biomateriais.
2.1 Carbonato de Cálcio
Para este trabalho de pesquisa utilizou-se como precursor o carbonato de cálcio 𝐶𝑎𝐶𝑂3 na forma de pó, fornecido pela LabMaster Ltda, lote n° 35216, com concentração de 99%. Este foi calcinado a 900ºC/3h, com objetivo de se obter o pó óxido de cálcio, conforme mostra a equação 3, que descreve a decomposição do carbonato de cálcio 𝐶𝑎𝐶𝑂3 com a liberação dióxido de carbono (𝐶𝑂2 – na fase gasosa) e obtenção do óxido de cálcio, este foi utilizado para síntese dos pós de fosfatos de cálcio hidratados.
𝐶𝑎𝐶𝑂3→ 𝐶𝑎𝑂𝑠+ 𝐶𝑂2↑𝑔
(Equação 3)
2.2 Ácido Fosfórico
2.3 Síntese do Fosfato de cálcio hidratado e obtenção da Matriz Hidroxiapatita Nanoestruturada
Os precursores utilizados para síntese do fosfato de cálcio hidratado foram o pó de óxido de cálcio 𝐶𝑎𝑂 , obtido da calcinação do carbonato de cálcio 𝐶𝑎𝐶𝑂3 à temperatura de 900ºCC/3h e a solução de ácido fosfórico. O método de síntese utilizado foi via úmida pela reação de dissolução-precipitação envolvendo fase sólida/líquida de 𝐶𝑎𝑂 e a solução de ácido fosfórico suficientes para se obter a razão 𝐶𝑎 𝑃= 1,67 molar.
O método de síntese foi realizado com a suspenção do pó de 𝐶𝑎𝑂 em meio litro de água destilada. Esta suspensão permaneceu sob agitação por 2 horas com objetivo de se obter a melhor dissociação iônica dos elementos dentro da solução coloidal. Durante este período realizaram-se medidas do valor do pH da suspensão coloidal. Depois das duas horas, adicionou-se, gota a gota, a solução de ácido fosfórico, mantendo-se a realização de medidas do valor do pH a cada 15 minutos. O gotejamento ocorreu a uma taxa de 2,5 mL/min. Toda a suspensão coloidal permaneceu sob agitação mecânica por 24 horas.
Após as 24 horas a solução foi seca, utilizando um evaporador rotativo, moída e peneirada em malha 100 µm ABNT. O material recuperado do peneiramento foi denominado de pó de fosfato de cálcio hidratado. Este foi posteriormente calcinado à temperatura de 900ºC/2h dentro da câmara de um forno tipo mufla marca HERAEUS - Instruments. O pó recuperado do forno à temperatura ambiente (25ºC), foi denominado de pó de hidroxiapatita nanoestruturada.
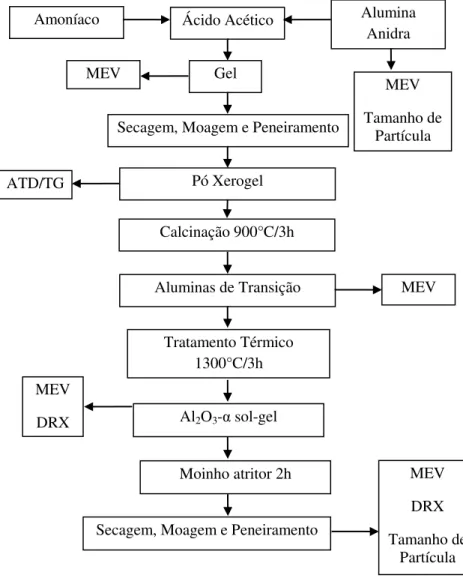
A figura 9 apresenta o fluxograma representativo do método utilizado para síntese e caracterização do pó nanoestruturados de fosfato de cálcio hidratado e de hidroxiapatita.
2.4 Processo Sol-Gel para Obtenção da Alumina-α
Figura 9 - Fluxograma representativo do processo de síntese da hidroxiapatita.
Fonte: produção do próprio autor.
sólido/liquido, dissolução/precipitação, formação de uma nova fase através da variação do valor do pH da suspensão coloidal ou da temperatura.
CaCO3
Calcinação 900°C/3h
CaO + H2O
Agitação Mecânica por 22h
Secagem, Moagem e Peneiramento Agitação Mecânica por 2h
Monitoramento do pH
Tamanho de partícula MEV
DRX
ATD/TG
Calcinação 900°C/2h
Hidroxiapatita Adição de H3PO4 + H2O
MEV
DRX
FTIR
Tamanho de partícula Monitoramento
do pH
MEV
ATD/TG
DRX
O processo sol-gel foi utilizado neste trabalho com objetivo de se obter alumina- de alta pureza, a qual foi utilizada como segunda fase na elaboração dos pós nanocompósitos de
𝐻𝐴 𝐴𝑙2𝑂3− 𝛼 sol-gel. O processo empregado para obtenção da
alumina- sol-gel seguiu o protocolo já utilizado por [SOUZA, 2009, PASSONI, 2010].
Utilizou-se o precursor pó Disperal P3 de alumina anidra e solução de ácido acético na concentração 1,6% em peso. O sol foi preparado pela adição do pó Disperal P3 à solução de ácido acético, sob agitação mecânica intensiva de aproximadamente 900 rpm mantida por 20 min. Após, adicionou-se gota a gota a solução de 𝑁𝐻4𝑂𝐻, na concentração 4𝑁 dentro da solução sol de alumina até sua gelificação. Este gel foi seco em estufa à temperatura de 120oC por 24 h. O material recuperado da estufa se apresentou na forma de aglomerados, sendo denominado de xerogel. Este passou pelo processo de moagem almofariz/pistilo e peneiramento na malha 100 µm ABNT, fornecendo o pó xerogel de alumina. Este pó foi submetido à calcinação em um forno tipo mufla à temperatura de 900ºC por 3 h, fornecendo as aluminas de transição , e . O pó formado pelas aluminas de transição foi submetido ao tratamento térmico à temperatura de 1300°C por 3 h para formação da fase 𝐴𝑙2𝑂3− 𝛼 sol-gel nanoestruturada.
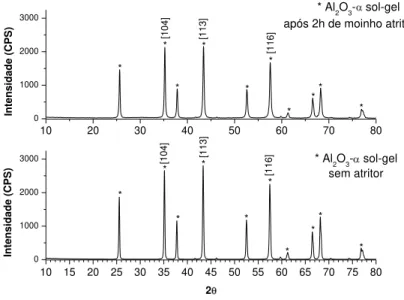
O pó de 𝐴𝑙2𝑂3− 𝛼 sol-gel foi submetido ao processo de fragmentação mecânica em moinho atritor de alta energia. O processo em moinho atritor ocorreu dentro de uma jarra de zircônia com uma concentração sólido/líquido de 50/50% em volume. Para se obter melhor eficiência durante o processo de moagem, utilizaram-se esferas de zircônia de diâmetro de 2,00 mm e álcool etílico. O material recuperado da moagem em moinho atritor passou pelo processo de secagem em evaporador rotativo, conforme já descrito anteriormente.
Figura 10 - Fluxograma representativo do processo de síntese e caracterização da alumina-α.
Fonte: produção do próprio autor.
Ácido Acético
MEV
DRX
Gel
Secagem, Moagem e Peneiramento
Aluminas de Transição
Tratamento Térmico 1300°C/3h Pó Xerogel
MEV
Al2O3-α sol-gel
Moinho atritor 2h Calcinação 900°C/3h
Secagem, Moagem e Peneiramento
MEV
DRX
Tamanho de Partícula
Amoníaco Alumina
Anidra
MEV
MEV
Tamanho de Partícula
2.5 Elaboração dos Pós Nanoestruturados
Foram elaboradas cinco composições de pós nanoestruturados, sendo uma composição a matriz cerâmica de hidroxiapatita (matriz óssea), depois os pós nanocompósitos com 1%, 2%, 3% e 5%, em volume de 𝐴𝑙2𝑂3− 𝛼 sol-gel.
A elaboração dos pós nanoestruturados foi realizada com ajuda de um moinho atritor de alta energia marca NETZSCH. Este método permitiu obter melhor dispersão da segunda fase alumina-α nanométrica na matriz hidroxiapatita. O processo de mistura das fases em moinho atritor foi realizado com uma razão sólido/líquido de 50%/50% em volume, por um período de duas horas, conforme descrito pelos autores
[CAMARGO, 2012, DELIMA, 2009]. Com objetivo de se obter a melhor eficiência no processo de moagem utilizou-se esferas de zircônia com diâmetro de 2,00 mm e álcool etílico. A suspensão coloidal recuperada do moinho atritor foi seca em evaporador rotativo fornecendo os pós nanoestruturados de hidroxiapatita e nanocompósitos. A figura 11 mostra o esquema geral de elaboração e caracterização dos pós nanocompósitos.
Figura 11 - Fluxograma representativo do processo de elaboração e caracterização dos pós nanoestruturados.
Fonte: produção do próprio autor. Matriz HA
MEV
DRX
Tamanho de partícula Moinho atritor 2h
Secagem e Obtenção do Pó Nanocompósito
2.6 Compactação e Sinterização
Os pós nanoestruturados recuperados do processo em moinho atritor, depois de secos e peneirados na malha # 100 m, foram introduzidos dentro de uma matriz metálica com dimensões 30 mm de largura, 70 mm de comprimento e 5 mm de altura. As paredes da matriz metálica foram protegidas com pó de estearato de zinco com objetivo de minimizar os esforços de cisalhamento na interface matriz/compactado e facilitar a desmoldagem dos corpos de prova. O processo de compactação dos pós nanoestruturados foi realizado em uma máquina universal de ensaios mecânicos, marca EMIC, modelo DL30000, sendo a carga de compactação utilizada de 30 MPa, com deslocamento da travessa de compactação de 0,1 mm/minuto.
Após o desmolde os corpos de prova foram cuidadosamente colocados dentro da câmara de um forno da marca Linberg/Blue e submetidos à sinterização a temperatura de 1250°C por 2 horas, com taxa de aquecimento da câmera do forno de 5°C/min. O processo de sinterização ocorreu dentro de uma atmosfera oxidante, ou seja, natural.
Os corpos de prova recuperados da sinterização se apresentaram com forma de placas retangulares com dimensões variadas.
2.7 Preparação dos Corpos de Prova para os Ensaios Mecânicos
2.8 Caracterização Morfológica e Microestrutural
As caracterizações morfológica e microestrutural foram realizadas com ajuda de um microscópio eletrônico de varredura, marca ZEISS, modelo DSM 940A, através do sistema de elétrons secundários (SE) e distância de objeto de 10 mm. Estes estudos foram realizados sobre os pós: carbonato de cálcio, alumina- sol-gel, fosfato de cálcio hidratado, hidroxiapatita e pós nanoestruturados recuperados do moinho atritor, de hidroxiapatita e nanocompósitos 𝐻𝐴 𝐴𝑙2𝑂3− 𝛼 sol-gel 1%, 2, 3 e 5% em volume. Esta técnica também ajudou na caracterização da microestrutura dos biomateriais recuperados da sinterização à temperatura de 1250ºC/2h: hidroxiapatita e nanocompósitos
𝐻𝐴 𝐴𝑙2𝑂3− 𝛼 sol-gel 1%, 2, 3 e 5% em volume.
2.9 Caracterização Física por Difratometria de Raios X (DRX)
A difratometria de raios X (DRX) serviu de apoio na caracterização cristalográfica, realizado com ajuda de um difratômetro de raios X (DRX) marca SHIMADZU, modelo X-RAY DIFFRACTOMETER LAB X XRD-6000, com anti-catodo tubo de cobre. Para obtenção dos difratogramas de raios X, utilizou-se uma tensão de 40 kv e intensidade de corrente de 30 mA, sendo o intervalo angular de varredura de 10° a 80°, com deslocamento do goniômetro de 2º/min em função de 2θ. Os estudos de caracterização física por DRX foram realizados desde o carbonato de cálcio utilizado para obtenção do 𝐶𝑎𝑂, sobre o pó de hidroxiapatita obtida da calcinação, alumina-α, pós nanoestruturados obtidos do moinho atritor e corpos de prova obtidos da sinterização.
2.10 Caracterização Química por Espectroscopia de Infravermelho por Transformada de Fourier (FTIR)
identificar as bandas vibracionais dos grupamentos 𝑂𝐻− e 𝑃𝑂
43− dentro das composições de fosfatos de cálcio. Os estudos foram realizados em um equipamento Perkin Elmer Spctrum, com refletância atenuada, utilizando intervalo de 4000 a 520 cm-1 com resolução de 4,00 cm-1. As análises por espectroscopia de Infravermelho foram realizadas sobre os pós: fosfato de cálcio hidratado, hidroxiapatita nanoestruturada e nanocompósitos recuperados do moinho atritor.
2.11 Análise do Tamanho de Partículas
Para a determinação do tamanho de partículas para as diferentes composições de pós nanoestruturados, utilizou-se o método de difração a laser. Este estudo foi realizado com ajuda do analisador de partículas marca SHIMADZU modelo SALD-7001, com laser semicondutor azul-violeta 𝛾= 405 𝑛𝑚 , o qual permite a determinação de tamanho de partículas de 10 nm a 500 µm. A determinação do tamanho de partícula foi realizada para os pós: fosfato de cálcio hidratado, alumina-α, hidroxiapatita e nanocompósitos recuperados do moinho atritor.
2.12 Area Superficial
𝐴𝑆=
6000
𝐷𝑎 ∙ 𝐷 ∙ 𝑓𝐺 (Equação 4)
Sendo:
𝐴𝑆 = área superficial das partículas (m2/g);
𝐷𝑎 = densidade teórica do material (g/cm3);
𝐷 = diâmetro médio das partículas (nm);
𝑓𝐺 = fator Gaussiano, utilizado como uma correção normalizada da
superfície de área. Para o caso dos fosfatos de cálcio, o 𝑓𝐺 utilizado é de
0,936243.
O diâmetro médio das partículas utilizado na equação 5 pode ser obtido pela análise de tamanho médio de partículas obtido por difração à laser.
A área superficial de grãos e/ou de partículas são grandezas significativas, quando se trata de desenvolvimento de biomateriais nanoestruturados, estes valores podem apresentar um diferencial sobre a molhabilidade, capilaridade e adesão celular na superfície das partículas e /ou grãos, o que poderá melhorar os processos de reparação e formação óssea [CAMARGO, 2012, CAMARGO, 2009 (a); SILVA, 2007].
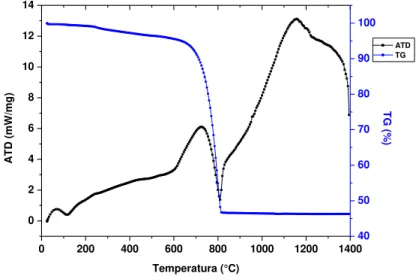
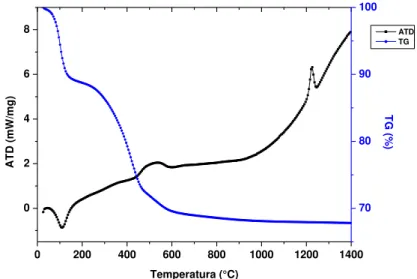
2.13 Análise Térmica Diferencial (ATD) e Termogravimetria (TG)