REVISTA
BRASILEIRA
DE
ANESTESIOLOGIA
PublicaçãoOficialdaSociedadeBrasileiradeAnestesiologiawww.sba.com.br
ARTIGO
CIENTÍFICO
Efeito
de
dexmedetomidina
sobre
lesão
pulmonar
aguda
em
modelo
experimental
de
isquemia-reperfusão
Ömer
Burak
Küc
¸ükebe
a,
Deniz
Özzeybek
b,
Ruslan
Abdullayev
a,∗,
Adil
Ustao˘
glu
c,
Is
¸ıl
Tekmen
de
Tuncay
Küme
eaAdıyamanUniversityResearchandEducationalHospital,DepartmentofAnesthesiologyandReanimation,Adıyaman,Turquia bDokuzEylülUniversityMedicalFaculty,DepartmentofAnesthesiologyandReanimation, ˙Izmir,Turquia
cZonguldakAtatürkHospital,DepartmentofAnesthesiologyandReanimation,Zonguldak,Turquia dDokuzEylülUniversityMedicalFaculty,DepartmentofHistologyandEmbryology, ˙Izmir,Turquia eDokuzEylülUniversityMedicalFaculty,DepartmentofMedicalBiochemistry, ˙Izmir,Turquia
Recebidoem1demarçode2015;aceitoem17deagostode2015 DisponívelnaInternetem28desetembrode2016
PALAVRAS-CHAVE
Experimental; Dexmedetomidina; Lesãodereperfusão; Lesãopulmonar aguda
Resumo
Objetivo: Alesãodeisquemia-reperfusãoéumadasconsequênciasdaaplicac¸ãodotorniquete
emcirurgiasdeextremidades.Oobjetivodoestudofoideterminaroefeitodedexmedetomidina
emlesãopulmonaragudaapósmodeloexperimentaldeisquemia-reperfusãoemextremidade
inferiorderatos.
Métodos: VinteeoitoratosalbinosWistarforamrecrutadosapósaprovac¸ãodoComitêdeÉtica
ealocadosemquatrogrupos,cadaumcomseteindivíduos.OGrupo1(Sham)recebeuapenas
anestesia.OGrupo2(IR)foisubmetidoa3horasdeisquemiae3horasdereperfusãocomo
usodetorniqueteemextremidadeinferiorapósaaplicac¸ãodaanestesia.Osgrupos3(D-50)
e4(D-100)foramsubmetidosaosmesmosprocedimentosdoGrupo2,excetoporreceberem
50 e 100mg.kg−1 dedexmedetomidina, respectivamente, porviaintraperitoneal uma hora
antesdaliberac¸ãodotorniquete.AmostrasdesangueforamcoletadasparaanálisedeTNF-␣
eInterleucina-6(IL-6).Amostrasdetecidopulmonarforamcoletadasparaanálisehistológica.
Resultados: Nãohouvediferenc¸asignificativaquantoaosvaloressanguíneosdeTNF-␣eIL-6
entre osgrupos, enquanto osescores delesão em tecidos pulmonaresrevelaramdiferenc¸a
significativa.OsescoreshistológicosobtidosnoGrupo2foramsignificativamentemaioresdo
que osdos grupos1, 3e 4,com valores-pde 0,001para cadacomparac¸ão.Alémdisso, os
escoresdoGrupo1foramsignificativamentemenoresdoqueosdosgrupos3e4,comvalores-p
de0,001e0,011,respectivamente.Nãohouvediferenc¸asignificativaentreosgrupos3e4.
∗Autorparacorrespondência.
E-mail:[email protected](R.Abdullayev). http://dx.doi.org/10.1016/j.bjan.2016.09.004
Conclusão:Dexmedetomidinamostroueficácianareduc¸ãodelesãoemtecidopulmonar
indu-zidaporisquemia-reperfusãoexperimentalemratos,ocasionadaporaplicac¸ãodetorniquete
emextremidade.
©2016SociedadeBrasileiradeAnestesiologia.PublicadoporElsevierEditoraLtda.Este ´eum
artigoOpen Accesssobumalicenc¸aCCBY-NC-ND(
http://creativecommons.org/licenses/by-nc-nd/4.0/).
KEYWORDS
Experimental; Dexmedetomidine; Reperfusioninjury; Acutelunginjury
Effectofdexmedetomidineonacutelunginjuryinexperimental ischemia---reperfusionmodel
Abstract
Purpose:Ischemia-reperfusioninjuryisoneoftheconsequencesoftourniquetapplicationfor
extremitysurgery.Theaimofthestudywastoestablishtheeffectofdexmedetomidineonthe
acutelunginjuryfollowinglowerextremityexperimentalischemia---reperfusionmodelinrats.
Methods:Twenty-eightWistar-AlbinobreedratswererecruitedafterEthicsCommittee
appro-valandallocatedinto4groups,eachwith7subjects.Group1(SHAM)receivedonlyanesthesia.
Group2(IR)hadexperienced3hofischemiaand3hofreperfusionusingleftlowerextremity
tourniquetafteranesthesiaapplication.Groups3(D-50)and4(D-100)hadundergonethesame
proceduresasintheGroup2,exceptforreceiving50and100mg.kg−1,respectively,
dexme-detomidineintraperitoneally1hbeforethetourniquetrelease.Bloodsampleswereobtained
fortheanalysisoftumornecrosingfactor-␣andinterleukin-6.Pulmonarytissuesampleswere
obtainedforhistologicalanalysis.
Results:Nosignificantdifferenceregardingbloodtumornecrosingfactor-␣andinterleukin-6
valueswasfoundamongthegroups,whereaspulmonarytissueinjuryscoresrevealedsignificant
difference.HistologicalscoresobtainedfromtheGroup2weresignificantlyhigherfromthose
intheGroups1,3and4withp-values0.001foreachcomparison.Moreover,Group1scores
werefoundtobesignificantlylowerthanthoseintheGroups3and4withp-values0.001and
0.011,respectively.NosignificantdifferencewasobservedbetweentheGroups3and4.
Conclusion:Dexmedetomidine is effective in reduction of the experimental
ischemia---reperfusioninducedpulmonarytissueinjuryinrats,formedbyextremitytourniquet
application.
©2016SociedadeBrasileiradeAnestesiologia.PublishedbyElsevierEditoraLtda.Thisisan
openaccessarticleundertheCCBY-NC-NDlicense(
http://creativecommons.org/licenses/by-nc-nd/4.0/).
Introduc
¸ão
Asuspensãodofluxo sanguíneo,istoé, isquemiatecidual, e a reperfusão após um período de tempo são os princi-paismecanismosfisiopatológicosresponsáveis porlesionar órgãos após alguns procedimentos médicos, como trans-plantedeórgãos,isquemiacerebral,acidentevascular cere-bral, infarto do miocárdio, tromboembolismo, circulac¸ão extracorpórea e cirurgias vasculares, grande traumatismo e choque hemorrágico, bem como procedimentos cirúrgi-coscom o usodetorniquete.1,2 Alesão isquêmica resulta
principalmente da necrosecelular devido à suspensão de oxigênio. Ofornecimento de oxigênio durante a isquemia não é suficiente para satisfazer as necessidades metabó-licas das células e essa condic¸ão resulta na ativac¸ão do metabolismoanaeróbico.3Quandoofluxosanguíneoretorna
novamenteaotecido,istoé,quandoareperfusãoteminício, oretornodofluxoparadoxalmenteaumentaodanoaos teci-doslocais,juntamentecomarespostainflamatória,oque resultaemdanosaórgãosdistantes.2,3Muitosagentes
infla-matóriosdemonstraram ser responsáveispor esses danos, entreelesalesãodeisquemia-reperfusão(LIR).2
Ascitocinasforamresponsabilizadaspordanosaórgãos distantesdevidoàLIR.4Relatou-seque osníveis
plasmáti-cos dofator-␣ denecrosetumoral (TNF-␣),interleucina-1 (IL-1) e IL-6estavam elevados em tecido renal e pulmo-nar após isquemia em membroposterior.5 Osmediadores
liberadosapósisquemia-reperfusão(IR)resultamemlesões orgânicaslocais edistantespormeioderadicaislivres de oxigênioe leucócitos.6,7Efeitos imunorreguladores
negati-vos denoradrenalinaforamdemonstradosnaformac¸ãode mediadoresdeorigemmonocítica/macrofágica(TNF-␣, IL-1,IL-6)eessesefeitosestavamligadosaadrenorreceptores e␣2.8
Dexmedetomidinaéumagonista␣2-adrenérgicopotente eseletivo,od-isômerofarmacologicamenteativoda mede-tomidina, que é metabolizado no fígado. Seu uso foi aprovado para sedac¸ão em unidade de terapia intensiva e tem propriedades sedativas e analgésicas.9,10 Há
pou-cosestudosnaliteraturasobreosefeitosanti-inflamatórios dedexmedetomidina.11---16Yagmurduretal.14demonstraram
tenhasidodemonstrado quedexmedetomidinatemalguns efeitosprotetoresem LIRlocalizada,nãoencontramosum estudodeseusefeitossobrearespostainflamatória sistê-micaedanosemórgãosdistantes.
Nossoobjetivofoiavaliarosefeitosdeduasdoses dife-rentesdedexmedetomidinasobrealesãopulmonaraguda apósmodeloexperimentaldeisquemia-reperfusãoem mem-bros inferiores de ratos. A hipótese teve como base os possíveisefeitosprotetoresdedexmedetomidinaelevouem considerac¸ãoseusefeitosanti-inflamatórios.
Métodos
EsteestudofoiconduzidonoLaboratóriodeExperimentac¸ão Animal da Faculdade de Medicina da Universidade Dokuz Eylul entre 01/01/2009 e 31/05/2009, após obter a aprovac¸ão doComitêdeÉticapara EstudosExperimentais emAnimaisdaUniversidadeDokuzEylul,Esmirna,Turquia (24/11/2008, n◦ 134, Presidente Prof. M. Olguner). Vinte
eoitoratos, fêmeasadultas,darac¸aWistar-Albino,entre 250-340g, foramusados para o estudo. Osanimais foram alimentadoscomrac¸ãopadrãoeáguaemantidosemciclos de12horasdeclaro/escuroparaadaptac¸ãoantesdoinício doestudo.Temperaturaeumidadetambémforam padroni-zadas.
Osratosforammantidosemjejumpor12hantesdo pro-cedimentocirúrgico, receberamsomente água. Cadarato foi pesado antes da experiência e as doses de dexmede-tomidina foramcalculadas.A distribuic¸ão dos animaisem quatro grupos foi feita de modo aleatório com o método deenvelopelacrado:Grupo1(Sham,n=7)recebeuapenas anestesia,comobtenc¸ãodeamostradesanguenaprimeira horade reperfusãoe amostras desangue e tecidono fim dareperfusão;Grupo 2s (IR, n=7) foisubmetidoa 3h de isquemiae3hdereperfusãoeusoutorniqueteemmembro posterioresquerdoapósaaplicac¸ãodaanestesia.Amostras desangueforamcolhidasnaprimeirahoradereperfusãoe amostrasde sanguee tecido nofimdareperfusão;Grupo 3(D-50,n=7)foisubmetidoaosmesmosprocedimentosdo Grupo2,excetoporreceber50g.kg---1dedexmedetomidina (Precedex, Abbott Laboratories Ltd., North Chicago ABD, 100g.mL---1)porviaintraperitoneal1hantesdaliberac¸ão do torniquete; Grupo 4 (D-100, n=7) foi submetido aos mesmos procedimentos do Grupo 2, exceto por receber 100g.kg---1dedexmedetomidinaporviaintraperitoneal1h antes da libertac¸ão do torniquete. Novamente, amostras desangueforamobtidasnaprimeirahoradereperfusãoe amostrasdesanguee tecidonofim dareperfusãoparaos grupos3e4.
Aanestesiafoiadministradaporviaintraperitonealcom mistura de50mg.kg−1decetamina (PfizerPharmaGmbH, Alemanha) e 10mg.kg−1 de cloridrato de xilazina (Alfa-zine,2%,Egevet).Aisquemiafoifeitacomgarroteelástico (1cmdelargurae30cmdecomprimento)aplicadoàregião inguinal do membro posterior esquerdo. O torniquete foi liberadopara estabelecerareperfusão após operíodo de tempodeterminado.Atemperatura ambientefoimantida estável,amesadeoperac¸ãofoiaquecidaparaprotegeros ratosdehipotermiae atemperaturacorporal dosanimais foimantidaentre36,8◦Ce37,5◦C.Osratosforam
hidrata-doscom3mL.kg---1.h---1decloretodesódioisotônico,porvia
subcutânea,durantetodooprocedimentodeIRparaevitara desidratac¸ão.Osanimaisforamsacrificadosapósaobtenc¸ão dasamostrasdesangueetecido.Adurac¸ãodoprocedimento foiigualemtodososgrupos.
No fimda primeira hora dastrês horas de reperfusão, 1,5mL de sangue foi coletado da veia da cauda dos ani-masparaanálisedeTNF-␣eIL-6,colocadoemtuboestéril comácidoetilenodiaminotetracético(EDTA)ecentrifugado por10min a umavelocidade de1.200rpm.O plasma das amostrasdesanguefoiseparadoecolocadoemtubos Eppen-dorf,congeladoemantidoa70◦Catéodiadaanálise.Os
ratosreceberamcloretodesódioisotônicoporvia intrape-ritoneal,emquantidadeigualàextraídaparaamostragem. No fim da reperfusão, o tórax foi aberto por abordagem subdiafragmática.Aamostrade sanguepara TNF-␣ e IL-6 foi obtida em volume de 2mL diretamente docorac¸ão e acondicionadadamesmaformamencionadaacima.Nofim doprocedimento,5mLdeformola10%foramlentamente aplicadosatravésdoápexcardíacocomumadaagulhade calibre 20G e o corac¸ão e o leito pulmonar foram exci-sados após o sacrifício. Uma secc¸ão da zona média do pulmãodireitoetodoopulmãoesquerdoforamcolocados em formol a 10% e mantidos parafixac¸ão por no mínimo 24h.
Análisedemediadoresinflamatórios
Aanálisedosmediadoresinflamatórios(TNF-␣vs.IL-6)foi realizadacomotesteElisa(Enzyme-LinkedImmunosorbent Assay).Osvaloresdeabsorbânciaforamlidosa450nmno dispositivoparaElisa(OrganonTechnicaMicropoc¸osSystem Reader230S).Osresultadosforamexpressosempg.mL---1.
Análisehistopatológica
Os tecidos pulmonares obtidos dos animais foram cora-doscomométodohematoxilina-eosina eexaminadoscom microscópiodeluz(OlympusBH-2)emampliac¸ãode200×. Seisregiõesaleatóriasforamselecionadasdecadaamostra eumaclassificac¸ãode0-4pontosfoifeita.Levaram-seem considerac¸ãoosachadoshistopatológicos,comohemorragia intersticialealveolar,infiltradodeneutrófilosintersticiale alveolar, edema e atelectasia. A classificac¸ão foi feitade acordocom a proporc¸ão daárea lesionada:0 = nenhuma lesão;1=<25%delesão;2=25-50%delesão;3=50-75% delesão;4=lesãodifusa.
Análiseestatística
OsdadosobtidosforamavaliadoscomoprogramaSPSS11.0 (Statistical Package for Social Sciences,Chicago, Illinois). OstestesdeKruskall-Wallisedoqui-quadradoforamusados paracomparar os grupos. O teste Ude Mann-Whitney foi usadoparacompararosgruposseparadamenteeacorrec¸ão de Bonferroni foi usada quando necessário. Valores de p
Grupo 1 (
SHAM
)
∆
---
-
---
-
--- n = 7
6. horas
4. horas
3. horas
0. hora
6. horas
4. horas
3. horas
0. hora
6. horas
4. horas
3. horas
2. hora
2. horas
0. hora
6. horas
4. horas
3. horas
0. hora
Histopatologia e
Bioquímica
Bioquímica
Histopatologia e
Bioquímica
Bioquímica
Histopatologia e
Bioquímica
Bioquímica
Grupo 2 (IR)
ISCHEMIA REPERFUSION
∆
---
-
---
-
--- n=7
Grupo 3 (D 50)
ISCHEMIA REPERFUSION
∆
---
-
--- --- n=7
Dexmedetomidina
50 µg.kg
–1Histopatologia e
Bioquímica
Bioquímica
Dexmedetomidina
100 µg.kg
–1Grupo 4 (D 100)
ISCHEMIA REPERFUSION
∆
---
-
---
--- n=7
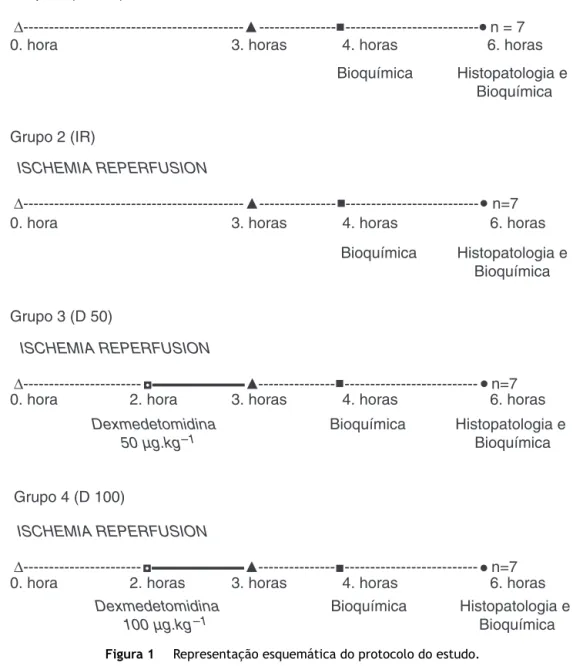
Figura1 Representac¸ãoesquemáticadoprotocolodoestudo.
Resultados
Esteestudofoiconcluídocom28ratos,cadagrupocomsete. Ointervalodetempoparaoestudofoiomesmodescritona sec¸ãoMétodos(fig.1).
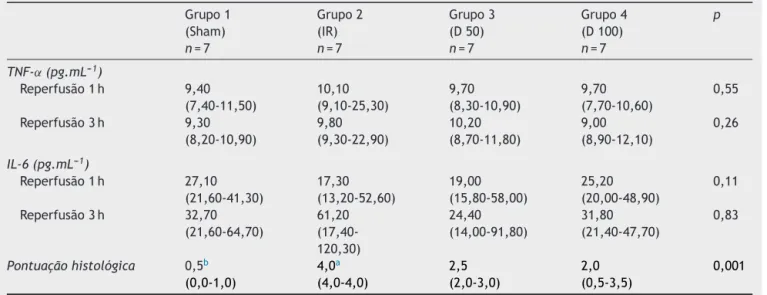
A tabela 1 mostra os valores de TNF-␣ e IL-6 e as classificac¸ões histológicas do tecido pulmonar. A análise intergrupos não revelou diferenc¸a estatisticamente signi-ficativa em relac¸ão aosvaloresde TNF-␣ e IL-6, tanto na primeiraquantonaterceirahoradereperfusão.
Aanálise estatísticadasalterac¸ões histológicas pulmo-nares foi feita com os valores médios das classificac¸ões obtidas a partir de seis áreas microscópicas examinadas. Houvediferenc¸aestatisticamentesignificativaentreos gru-posnaclassificac¸ãodaslesõespulmonares(p=0,001).Lesão difusa(classificac¸ão4)em todososespécimesdoGrupo2. Asclassificac¸õeshistológicasobtidasparaoGrupo2foram significativamente diferentes daquelas para os grupos 1, 3 e 4 (p=0,001 para cada comparac¸ão). Além disso, as
classificac¸õesdoGrupo1foramsignificativamentediferente daquelas dos grupos 3 e 4 (p=0,001e0,011, respectiva-mente). Nãohouve diferenc¸asignificativaentreosgrupos trêsequatro.
Tabela1 ValoresdeTNF-␣eIL-6epontuac¸õeshistológicas
Grupo1
(Sham)
n=7
Grupo2
(IR)
n=7
Grupo3
(D50)
n=7
Grupo4
(D100)
n=7
p
TNF-˛(pg.mL---1)
Reperfusão1h 9,40
(7,40-11,50)
10,10 (9,10-25,30)
9,70 (8,30-10,90)
9,70 (7,70-10,60)
0,55
Reperfusão3h 9,30
(8,20-10,90)
9,80 (9,30-22,90)
10,20 (8,70-11,80)
9,00 (8,90-12,10)
0,26
IL-6(pg.mL---1)
Reperfusão1h 27,10
(21,60-41,30)
17,30 (13,20-52,60)
19,00 (15,80-58,00)
25,20 (20,00-48,90)
0,11
Reperfusão3h 32,70
(21,60-64,70)
61,20 (17,40-120,30)
24,40 (14,00-91,80)
31,80 (21,40-47,70)
0,83
Pontuac¸ãohistológica 0,5b
(0,0-1,0)
4,0a
(4,0-4,0)
2,5 (2,0-3,0)
2,0 (0,5-3,5)
0,001
a Diferenc¸asignificativanoGrupo2,emcomparac¸ãocomosgrupos1,3e4,p<0,05. b Diferenc¸asignificativanoGrupo1,emcomparac¸ãocomosgrupos3e4,p<0,05.
Valoresexpressosemmediana(mínimo-máximo).
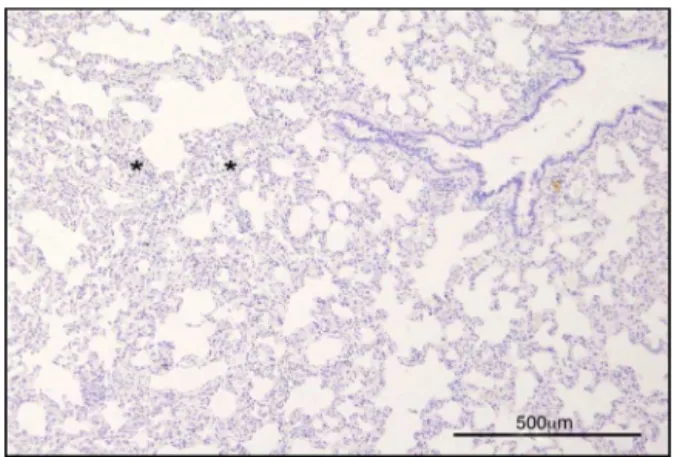
Figura2 Grupo1:estruturanormaldetecidopulmonar ven-tilado.
Figura3 Grupo2:aestruturaalveolarperdeuoseupadrão (↑), alterac¸õesenfisematosas (A),infiltrac¸ãode células infla-matóriasnoparênquima(P˙I).
Figura4 Grupo 2: infiltrac¸ão densade neutrófilos, alarga-mentodoparênquima,áreaspulmonaresnãoventiladas( )e áreasatelectásicas(A).
de neutrófilos no interstício, o espessamento de septos interalveolares,aatelectasia,acongestão,ahemorragiae oenfisemaforammenoresdoquenoGrupo2.Tecido pulmo-narnormalfoiobservadonasáreascontíguas,adespeitode levealargamentodoparênquima einfiltrac¸ão de neutrófi-los.Algumasregiõesapresentaramtecidopulmonarnormal juntamentecomhemorragiaparenquimatosaintensa,áreas enfisematosas e infiltrac¸ões peribrônquicas (fig. 5). No Grupo4,asamostrasapresentaramleveinfiltrac¸ãode neu-trófilosintersticial,espessamentodeseptosinteralveolares, atelectasia,congestãoehemorragiaemgraumuitoinferior doqueasamostrasdoGrupo2.Algumasregiões apresenta-ramtecidopulmonarcompletamentenormal(fig.6).
Discussão
Figura 5 Grupo 3: leve alargamento do parênquima e infiltrac¸ãodeneutrófilos(*),juntamentecomestruturatecidual pulmonarnormaladjacente.
Figura 6 Grupo 4: leve infiltrac¸ão inflamatória e espessa-mentodos septosinteralveolares (*),juntamentecomtecido pulmonarnormal.
induzida pela aplicac¸ão de torniquete em extremidade. Embora não tenha havido diferenc¸as entre os grupos em relac¸ãoaosníveisplasmáticosdosmediadoresinflamatórios TNF-␣ e IL-6, uma diferenc¸a significativa foi observada nas alterac¸ões histológicas dos tecidos. A classificac¸ão histológicadoGrupo2foielevada,indicouefeitosdalesão de IRno tecido pulmonar. Os grupos 3 e 4 apresentaram pontuac¸õesmenoresdelesão,indicaramefeitoprotetorde dexmedetomidinacontraaLIR.
Embora alguns autores oferec¸am múltiplos métodos de ligac¸ão em vez da aplicac¸ão de torniquete devido à preocupac¸ãocomaobstruc¸ãovenosaelinfáticaelesão mus-cularapósacompressãomecânicaprolongada,17 ométodo
deaplicac¸ãodetorniquetenãoéinvasivoeparecesermais práticonaaplicac¸ãoclínica.7,18
Diferentestemposdeisquemiaereperfusãoforam usa-dos para a induc¸ão de IR na literatura. Nós levamos em considerac¸ão a resistência do tecido contra a isque-mia.Por exemplo,alterac¸õesmorfológicasimportantesno tecidomuscular surgem após 2h deisquemia e, porisso, estudosque avaliaram tecidos musculares em LIR usaram temposmaislongosdeisquemia.19,20Umacorrelac¸ão
impor-tante entre o tempo de isquemia e a lesão isquêmica foiobservada.21 Considerando osrelatos delesão
histoló-gica irreversível20 e de infiltrac¸ão difusa de neutrófilos18
no tecidomuscular após 3h de isquemia em estudos que avaliaramaLIRemtecidomuscular,optamosporumtempo deisquemiade3hemestudo.
Observou-seque o tempodereperfusãotambémé um fator importante na formac¸ão dos efeitos locais e
distan-tes da IR.2,7,19 Yasin et al.7 usaram tempos diferentes de
reperfusãoapós 3hdeisquemiae descobriramcorrelac¸ão positiva entre o tempo de reperfusão e as disfunc¸ões orgânicas distantes. Também descobriram alterac¸ões his-tológicas após 3h de reperfusão que nãoeram aparentes nas primeiras 2h. Portanto, optamos por um tempo de reperfusão de 3h. Alterac¸ões histológicas proeminentes, comoinfiltrac¸ãodifusadeneutrófilos,distorc¸ãoda sequên-cia alveolar e edema no tecido pulmonar do grupo IR, sustentaram a nossa opc¸ão. Essesachados estão em con-formidade com os de estudos que usaram os mesmos tempos.7,18
TNF-␣mostrouterumpapel importantenapatogênese da síndrome de resposta inflamatória sistêmica (SRIS) e falênciademúltiplosórgãos(FMO).5,22,23Mecanismos
seme-lhantesforamsugeridosnosefeitoslocaisedistantesdaLIR e estudosmostraramqueTNF-␣desempenhaumpapelna patogênesedalesãoorgânica.3,7Similarmente,IL-6também
mostroudesempenharumpapelnareac¸ãoinflamatória com-plexaassociadaaotrauma,choqueeinfecc¸ão.24Correlac¸ão
positiva foi demonstrada entre as concentrac¸ões plasmá-ticas de IL-6e a magnitudeda lesãoem tecidos moles.24
EstudosqueavaliarammodelosdeIRemextremidades pos-terioresmostraramumaumentodeIL-6emcorrelac¸ãocom TNF-␣.5,6Yasinetal.7sugeriram quearesposta
inflamató-ria relacionada àIRpodeser observadanos níveis séricos de TNF-␣ e IL-6 e que há correlac¸ão positiva entre esse aumentoelesõesdeórgãosdistantes.Osautoresavaliaram osníveissanguíneosdeTNF-␣eIL-6naprimeira,segundae terceirahoradereperfusãoapós3hdeisquemia. Descobriu--se que TNF-␣ aumentou deforma significativano fimda primeirahoraevoltouaosvaloresdecontrole nasegunda hora,enquantoosvaloresdeIL-6aumentaram progressiva-menteapósaprimeirahoradereperfusãocompiconofim daterceirahora.Portanto,avaliamososníveis sanguíneos deTNF-␣eIL-6,tantonofimdaprimeiraquantodaterceira hora.
Vários estudos clínicos e experimentais foram condu-zidos com dexmedetomidina devido às suas propriedades analgésicas, ansiolíticas e sedativas.25,26 Além disso,
demonstrou-se que dexmedetomidina tem propriedades anti-inflamatórias em estudos que avaliaram seus efeitos em modelosdeinflamac¸ãoisquêmicae tóxica.11 Taniguchi
etal.11demonstraramquedexmedetomidinaatenuaalesão
pulmonarediminuiastaxasdemortalidadeaodiminuiros níveisdeTNF-␣eIL-6eainfiltrac¸ãodeneutrófilosnas pare-desalveolaresemmodeloexperimentaldechoque séptico eendotoxêmico.Shen etal.27 avaliaramosníveis de
TNF--␣ e IL-6em lesãopulmonar em modelo experimental de LIR intestinal e descobriram diminuic¸ão daproduc¸ão des-sas citocinas notecidopulmonarapós a administrac¸ão de dexmedetomidina.
Dexmedetomidinafoi administrada por via intraperito-neal antes28 ou durante12-14 a IR em modelos de IR em
comparem os tempos de aplicac¸ão. Além disso, alguns estudos que avaliaram os efeitos de dexmedetomidina administradaintraperitoneal mostraramqueostemposde IRnãoforammaislongosdoque ostemposdeeliminac¸ão dedexmedetomidina.13,28Comooprincipalresponsávelna
formac¸ão delesãopulmonaréoprocesso dereperfusãoe osníveisdeTNF-␣comec¸amasubirpertodofimda isque-mia---comníveisdepiconaprimeirahoradereperfusão---,7
consideramosrelevanteadministrardexmedetomidinauma horaantesdareperfusão.
Nãoencontramosintervaloscertosdadosede dexmede-tomidinaparaseusefeitosanti-inflamatóriosnaliteratura.A dosededexmedetomidina,administradaporvia intraperito-neal,foiestabelecidaem100g.kg---1,adosemaiselevada administrada de formasegura na literaturaatual,16,28 e a
segundadose foiestabelecida em 50g.kg---1, paraavaliar seuspossíveisefeitosadependerdadose.
AdespeitodetempossemelhantesdeIRem estudosde LIR pulmonar após aplicac¸ão de torniquete em membros de ratos, resultados diferentes em relac¸ão aos níveis de TNF-␣ foram observados.5,18,29 Seekamp et al.5 relataram
que os níveis de TNF-␣ não foram detectados no sangue durante todo o tempode quatro horas deisquemia, mas comec¸aramaseelevarnaprimeirahoradereperfusãocom declínioapósasegundahora.Alémdisso,osníveis deIL-6 comec¸aram ase elevarnotrigésimominuto, compico no fimda quartahora.Yassinetal.7 relataram que osníveis
deTNF-␣ eIL-6atingemseuspicosna primeirae terceira hora de reperfusão, respectivamente; osníveis de TNF-␣ caíramabaixo dos níveis detectáveisapós asegunda hora dereperfusãoeIL-6atingiuníveisplasmáticosdetectáveis apartirdaprimeirahoradereperfusão.
Duru etal.,18 Harkin etal.30 e Gaines et al.31 usaram
modelos e tempos semelhantes de IR e, embora tenham observado alterac¸ões histopatológicas devido à LIR, não conseguiram observar alterac¸ões nos níveis de TNF-␣. De forma semelhante, Welbourn et al.29 não observaram
alterac¸õesnosníveisdeTNF-␣apósareperfusãoe concluí-ram que TNF-␣ desempenha um papel na patogênese da LIRporqueasalterac¸õeshistopatológicasdiminuíramcoma aplicac¸ãodeanti-TNF.Tambémnãoobservamosdiferenc¸as nos níveis de TNF-␣ e IL-6 nos grupos que receberam dexmedetomidina, em comparac¸ão com o grupo Sham, apesardasdiferenc¸ashistopatológicassignificativas.
Essacondic¸ãopodeseratribuídaaonúmeroinsuficiente deanimais.Duruetal.18 relataram quearazão pelaqual
não conseguiram demonstrar alterac¸ões no nível de cito-cinas foiporque eles podemnãoteratingido osníveis de picodeTNF-␣,poisobtiveramasamostrasdesanguenofim dasegundahoradereperfusão.Gainesetal.31 atribuíram
essacondic¸ãoàinsuficiência deamostrasdesangue. Wel-bournetal.29 propuseramqueTNF-␣ podepermanecerno
tecidoapósaproduc¸ãodemacrófagospulmonarese, por-tanto,nemsemprepoderiaserdetectadonosangue---TNF-␣ podemediaralesãotecidualpulmonareativaroendotélio localmente.
A LIRinduzida commodelo deaplicac¸ão detorniquete foi histopatologicamente demonstrada neste estudo. As alterac¸õesnoGrupoIRforamsignificativasemcomparac¸ão comoGrupoShameambososgruposdedexmedetomidina e isso demonstrou que o modelo foi conduzido de forma adequada. As diferenc¸as significativas nos resultados dos
gruposdedexmedetomidina,emcomparac¸ãocomoGrupo IR,foraminterpretadascomodexmedetomidinadiminuiua lesãopulmonar.
Embora as pontuac¸ões histopatológicas entre os gru-poscom dexmedetomidina(50 e 100g.kg---1)não tenham sidosignificativamentediferentes,algumasáreasdetecido pulmonarnormal ao examemicroscópico noGrupo D-100 sugeriram que o medicamento pode ter agido de forma dependentedadose.Estudoscomtamanhoamostralmaior ediferentesdoses,temposeviasdeadministrac¸ãopodem serconduzidosparaavaliaresseefeito.
Em conclusão,em nossoestudo de modelo experimen-taldeIRinduzidoportorniqueteem membroposteriorde ratos, dexmedetomidina foi eficaz na prevenc¸ão de lesão pulmonarinduzidaporIR.Asdiferenc¸ashistopatológicasnos níveisdeIL-6entreosdoisgruposcomdiferentesdosesde dexmedetomidina,emboranãosejaestatisticamente signi-ficativa,sugereafeituradeestudoscomamostrasmaiores paraavaliarosefeitosdedosesdiferentes.
Declarac¸ãodeimplicac¸ão
Este estudo experimental demonstra a capacidade da dexmedetomidina de reduzir a lesão relacionada à isquemia-reperfusãoexperimentalem ratos.Estudos clíni-coscontroladospodemserfeitosemhumanosparaobservar osignificadoclínicodesseefeito.
Conflitos
de
interesse
Osautoresdeclaramnãohaverconflitosdeinteresse.
Referências
1.CerraFB, LajosTZ,MontesM,etal.Hemorrhagicinfarction: areperfusion injuryfollowingprolonged myocardialischemic anoxia.Surgery.1975;78:95---104.
2.WelbournCR,GoldmanG,PatersonIS,etal.Pathophysiologyof ischaemiareperfusioninjury:centralroleoftheneutrophil.Br JSurg.1991;78:651---5.
3.Grace PA. Ischaemia-reperfusion injury. Br J Surg. 1994;81:637---47.
4.VilcekJ.Thecytokines:anoverview.In:ThomsonAW,editor. TheCytokineHandbook,vol.1,4thed.London:ElsevierScience
AcademicPress;2003.p.3---18.
5.Seekamp A, Mulligan MS, Till GO, et al. Requirements for tumor necrosis factor-alpha and interleukin-1 in limb ische-mia/reperfusioninjuryandassociatedlunginjury.AmJPathol. 1993;143:453---63.
6.SeekampA,TillGO,MulliganMS,etal.Roleofselectinsinlocal and remotetissueinjury followingischemiaand reperfusion. AmJPathol.1994;144:592---8.
7.Yassin MM, Barros D’Sa AA, Parks G, et al. Lower limb ischemia---reperfusion injury triggers a systemic inflamma-toryresponse and multipleorgandysfunction. World JSurg. 2002;26:115---21.
8.MaesM,LinA,KenisG,etal.Theeffectsofnoradrenalineand alpha-2adrenoceptoragentsontheproductionofmonocytic products.PsychiatryRes.2000;96:245---53.
9.VennRM,BryantA,HallGM,etal.PreliminaryUKexperience ofdexmedetomidineanovelagentforpostoperativesedation intheintensivecareunit.Anaesthesia.1999;54:1136---42. 10.Bhana N, Goa KL, McClellan KJ. Dexmedetomidine. Drugs.
11.Taniguchi T, Kidani Y, Kanakura H, et al. Effects of dexmedetomidine on mortality rate and inflammatory res-ponses to endotoxin-induced shock in rats. Crit Care Med. 2004;32:1322---6.
12.JolkkonenJ,PuurunenK,KoistinahoJ,etal.Neuroprotection bythealpha2-adrenoceptoragonist,dexmedetomidine,inrat focalcerebralischemia.EurJPharmacol.1999;372:31---6. 13.EserO,FidanH,SahinO,etal.Theinfluenceof
dexmedetomi-dineonischemicrathippocampus.BrainRes.2008;1218:250---6. 14.Yagmurdur H, Ozcan N, Dokumaci F, et al. Dexmedetomi-dine reducestheischemia---reperfusion injurymarkersduring upper extremity surgery with tourniquet. J Hand Surg Am. 2008;33:941---7.
15.YangCL,Tsai PS,Huang CJ. Effects ofdexmedetomidine on regulatingpulmonaryinflammationinaratmodelof ventilator--inducedlunginjury.ActaAnaesthesiolTaiwan.2008;46:151---9. 16.Kocoglu H, Ozturk H, Ozturk H, et al. Effect of dexme-detomidine on ischemia-reperfusion injury in rat kidney: a histopathologicstudy.RenFail.2009;31:70---4.
17.Tassiopoulos AP, Carlin RE, Gao Y, et al. Role of nitric oxide and tumor necrosis factor on lung injury caused by ischemia/reperfusion of the lower extremities. J Vasc Surg. 1997;26:647---56.
18.Duru S, Koca U, Öztekin S, et al. Antithrombin III pretre-atment reduces neutrophil recruitment into the lung and skeletal muscle tissues in the rat model of bilateral lower limbandreperfusion:a pilotstudy.ActaAnaesthesiolScand. 2005;49:1142---8.
19.KhalilAA,AzizFA,HallJC.Reperfusioninjury.PlastReconstr Surg.2006;117:1024---33.
20.Blaisdell FW. The pathophysiology of skeletal muscle ische-miaandthereperfusionsyndrome:areview.CardiovascSurg. 2002;10:620---30.
21.PetrasekPF,Homer-VanniasinkamS,WalkerPM.Determinants of ischemic injury to skeletalmuscle. JVasc Surg. 1994;19: 623---31.
22.Seal JB, Gewertz BL. Vascular dysfunction in ischemia--reperfusioninjury.AnnVascSurg.2005;19:572---84.
23.YaoYM,Sheng ZY,YuY,et al.Thepotentialetiologicroleof tumornecrosisfactorinmediatingmultipleorgandysfunction inratsfollowingintestinalischemia-reperfusioninjury. Resus-citation.1995;29:157---68.
24.RoumenRM,HendriksT,vanderVen-JongeKJ,etal.Cytokine patternsinpatientsaftermajorvascularsurgery,hemorrhagic shock,andsevereblunttrauma.Relationwithsubsequentadult respiratorydistresssyndromeandmultipleorganfailure.Ann Surg.1993;218:769---76.
25.KorogluA,DemirbilekS,TeksanH,etal.Sedative, haemody-namicandrespiratoryeffectsofdexmedetomidineinchildren undergoingmagneticresonanceimagingexamination: prelimi-naryresults.BrJAnaesth.2005;94:821---4.
26.ArainSR,RuehlowRM,UhrichTD,etal.Theefficacyof dexme-detomidineversusmorphineforpostoperativeanalgesiaafter majorinpatientsurgery.AnesthAnalg.2004;98:153---8. 27.Shen J, Fu G, Jiang L, et al. Effect of
dexmedeto-midine pretreatment on lung injury following intestinal ischemia---reperfusion.ExpTherMed.2013;6:1359---64. 28.Engelhard K, Werner C, Eberspacher E, et al. The effect
of the alpha 2-agonist dexmedetomidine and the N-methyl--d-aspartate antagonist S(+)-ketamine on the expression of apoptosis-regulatingproteinsafterincompletecerebral ische-miaandreperfusioninrats.AnesthAnalg.2003;96:524---31. 29.WelbournR,Goldman G,O’RiordainM,etal.Rolefor tumor
necrosisfactorasmediatoroflunginjuryfollowinglowertorso ischemia.JApplPhysiol.1991;70:2645---9.
30.HarkinDW,BarrosD’SaAA, McCallionK,etal.Ischemic pre-conditioningbeforelowerlimbischemia---reperfusionprotects againstacutelunginjury.JVascSurg.2002;35:1264---73. 31.GainesGC,WelbornMB3rd,Moldawer LL,etal.Attenuation