SOCIEDADE BRASILEIRA DE ORTOPEDIA E TRAUMATOLOGIA
w w w . r b o . o r g . b r
Artigo
Original
Avaliac¸ão
do
desempenho
in
vivo
de
pinos
porosos
de
hidrogel
para
preenchimento
de
defeito
osteocondral
em
coelhos
夽
Túlio
Pereira
Cardoso
a,∗,
André
Petry
Sandoval
Ursolino
a,
Pamela
de
Melo
Casagrande
a,
Edie
Benedito
Caetano
a,
Daniel
Vinicius
Mistura
be
Eliana
Aparecida
de
Rezende
Duek
a aPontifíciaUniversidadeCatólicadeSãoPaulo,FaculdadedeCiênciasMédicasedaSaúdedeSorocaba,Sorocaba,SP,BrasilbUniversidadeFederaldeSãoCarlos,Sorocaba,SP,Brasil
informações
sobre
o
artigo
Históricodoartigo:
Recebidoem14dejaneirode2016 Aceitoem29demarçode2016
On-lineem13dejulhode2016
Palavras-chave:
Cartilagemarticular Hidrogéis/química Coelhos
r
e
s
u
m
o
Objetivo:Trabalho experimentalparaavaliarodesempenho biológico dearcabouc¸os de hidrogelpoli(L-co-D,Lácidolático)-co-trimetilenocarbonato/poli(álcoolvinílico) (PLDLA--co-TMC/PVA)comoimplantenopreenchimento,enãonoreparo,dedefeitoosteocondral emcoelhosNovaZelândiaeverificarainfluênciadomaterialnaprotec¸ãotecidualinvivo.
Métodos:Foramusados12coelhosdivididosemgruposdenovee16semanas.Emcada animalfoicriadoumdefeitoosteocondralemambososcôndilosfemoraismediais,emum foiimplantadoumarcabouc¸odehidrogel(grupopino)enooutrofoimantidoodefeito(grupo controle).Apósosacrifíciodosanimais,foifeitaanálisehistológicadomaterial.
Resultados: Oscôndilosdogrupopinonãoevidenciaramreac¸ãoinflamatóriaeestavam rode-adosporcápsulafibrosa.Jánogrupocontrole,umamaiorproliferac¸ãoósseafoiobservada nasáreasdodefeito,porémcomcartilagemarticulardesorganizada,fibroseevidente,atrofia comexposic¸ãoósseaeproliferac¸ãodemembranasinovial.
Conclusão:Ospinosdehidrogelsãopromissoresnafunc¸ãodepreenchimentodedefeitos oste-ocondrais,nãoocasionam,demodogeral,reac¸ãoinflamatóriaenãosãoeficazesnoreparo
dedefeitososteocondrais.
©2016SociedadeBrasileiradeOrtopediaeTraumatologia.PublicadoporElsevierEditora Ltda.Este ´eumartigoOpenAccesssobumalicenc¸aCCBY-NC-ND(http:// creativecommons.org/licenses/by-nc-nd/4.0/).
夽
TrabalhodesenvolvidonoLaboratóriodeBiomateriais,FaculdadedeCiênciasMédicasedaSaúdedeSorocaba,PontifíciaUniversidade CatólicadeSãoPaulo,Sorocaba,SP,Brasil.
∗ Autorparacorrespondência.
E-mail:[email protected](T.P.Cardoso). http://dx.doi.org/10.1016/j.rbo.2016.03.011
In
vivo
evaluation
of
porous
hydrogel
pins
to
fill
osteochondral
defects
in
rabbits
Keywords: Articularcargilage Hydrogels/chemistry Rabbitsa
b
s
t
r
a
c
t
Objective: Thisexperimentalstudyaimedtoevaluatethebiologicalperformanceofpoly (L-co-D, L-lacticacid)-co-trimetilenecarbonate/poly(vinylalcohol)(PLDLA-coTMC/PVA), hydrogelscaffolds,asanimplantinthefilling(andnotintherepair)ofosteochondraldefects inNewZealandrabbits,assessingtheinfluenceofthematerialintissueprotectioninvivo.
Methods: Twelverabbitsweredividedintogroupsofnineand16weeks.Ineachanimal, an osteochondral defectwascreated inboth medialfemoral condyles.In one knee, a hydrogelscaffoldwasimplanted(pingroup)andintheother,thedefectwasmaintained (controlgroup).Ahistologicalanalysisofthematerialwasperformedaftereuthanasia.
Results: Thecondylesofthepingroupshowednoinflammatoryreactionandwere surroun-dedbyafibrouscapsule.Thecontrolgrouppresentedhigherbonegrowthintheareasofthe defect,butwithdisorganizedarticularcartilage,evidentfibrosis,boneexposure,atrophy, andproliferationofsynovialmembrane.
Conclusion:Thehydrogelpinsarepromisinginfillingosteochondraldefects,generallydonot causeinflammatoryreactions,andarenoteffectiveintherepairofosteochondraldefects.
©2016SociedadeBrasileiradeOrtopediaeTraumatologia.PublishedbyElsevierEditora Ltda.ThisisanopenaccessarticleundertheCCBY-NC-NDlicense(http:// creativecommons.org/licenses/by-nc-nd/4.0/).
Introduc¸ão
Aosteoartroseouosteoartriteéumadasafecc¸õesquemais acometemohomem.1Suaprevalênciaaumentacomopassar dosanos,é comumapós os60 anos.2 Acartilagem articu-lareoossosubcondralformamumsistemadelubrificac¸ão, estabilizac¸ão e distribuic¸ão uniforme de carga, absorvem choques epermitem movimentac¸ão com baixafricc¸ão por váriasdécadas.2–4 Dessaforma,acartilagemprotegeoosso subcondral de alto estresse e reduz a pressão normal de contato.2,5 Acartilagemdegradadaevoluicomdor,rigideze diminuic¸ão domovimentoarticular.Grac¸as àbaixa capaci-dadederegenerac¸ãocondral,aosteoartroseéumdosmais importantesproblemasnaortopedia.Comoaumentoda lon-gevidadehumanaedapráticaesportivanasúltimasdécadas observamoscadavezmaislesõesosteocondrais.2
Acartilagemarticularnormalapresentaumafasesólida constituídaprincipalmenteporcolágenoeproteoglicanos (15-32%) e umafase fluida composta predominantemente por água (68-85%).2 A cartilagem hialinacompõe-se de10% de células(condrócitos) edensamatrizextracelular,com 60 a 80%deágua,10a20%defibrasdecolágenotipoIIe10a15%de proteoglicanos.Aspropriedadesmecânicasdacartilagem arti-cularatornamcapazdetransmitircargadeaproximadamente oitovezesopesocorporal,grac¸asàexsudac¸ãoeaomovimento dofluídopelosporosdacartilagem,econferemumcoeficiente defricc¸ãode0,008(mi).4,6
Oossosubcondraléumafinacamadadeossodensoeduro emcontatocomacartilagemarticular,enquantooosso tra-becularécompostoporabundantematriz(fibrasdecolágeno eminerais)queagenatransmissãodecarga.6
Porseravascular,acartilagemdependedavascularizac¸ão proveniente da medula óssea para que ocorra migrac¸ão de células mesenquimais, responsáveis pelo processo de
cicatrizac¸ão.7,8 Alémdisso,aslesõessuperficiais da cartila-gemarticular,quenãoenvolvemoossosubcondral,têmpouca capacidadeintrínsecadereparac¸ão.9
Tantonaosteoartroseprimáriacomonasecundária,a car-tilageméotecidoquesofreasmaioresaberrac¸ões.Dentreas alterac¸õesmorfológicasocorremperdadesuanatureza homo-gênea,fragmentac¸ão,fibrilac¸ão,fissuraseulcerac¸ões.Coma progressãodadoenc¸a,ocasionalmentenãorestanenhumae áreasdeossosubcondralficamexpostas.10
Podemosconsiderartrêsfasesnoprocessoderegenerac¸ão tecidual: necrose, inflamac¸ão e reparo.11,12 Porém, a cicatrizac¸ão de lesão restrita à cartilagem hialina pode nãoocorrerdessaforma.13Lesõessuperficiaisdacartilagem hialina que não atinjam o osso subcondral tendem a não cicatrizar.9 Nessa lesão ocorre degenerac¸ão da cartilagem apartirda zonasuperficialeobservam-sefinasporc¸õesde fibras de colágeno com aspecto descamativo. Com a pro-gressão da lesão épossível visualizar fissuras verticais na cartilagem articular,queproduzemaspectoirregular esem brilho.4,14
Alesãocondraldesencadeariaumprocessoinflamatório eo hematomarapidamente seorganizariaemcoágulos de fibrina,glóbulosbrancoseelementosdamedulaóssea.
Célulasindiferenciadasdamedulaedoendotélio vascu-larsãotransformadasemfibroblastosprimitivosque,como aportedecapilaresecoágulosdefibrina,setransformamem tecidofibroblásticovascularizadodereparac¸ão.11Essetecido fibrocartilaginoso,adependerdosestímulosmecânicose bio-lógicos, formará umtecido cartilaginoso.13 A neoformac¸ão ósseamigradabasedodefeitoparaasuperfíciearticularna regiãoemcontatocomoossosubcondral. Umtecido fibro-cartilaginoso preenche azona de transic¸ão einterrompe a formac¸ãodetecidoósseo.4,11,14
sintetizaproteoglicanosdemenorpesomolecular.Comoas fibrasdecolágenodotipoIItêmmenordiâmetroedisposic¸ão mais irregular, esse arranjo favorece a permeabilidade à água. Essetecido neoformadoapresentamenor módulode elasticidade quandocomparado como tecido cartilaginoso normal.4,16,17
Otratamentocirúrgicodelesõescondraiseosteocondrais representaumgrandedesafio.Podemostentaraestimulac¸ão daformac¸ãodetecidocartilaginosooufibrocartilaginoso,que seriaareparac¸ãoouasubstituic¸ãodessaslesõesportecidos comcaracterísticassemelhantes.4,13
Não existem tecidos de substituic¸ão com propriedades mecânicassimilaresaotecidooriginal.18Pesquisascom enge-nhariadetecidoqueusasistemastridimensionaissintéticos comarcabouc¸osporosostêmsidofeitas.19,20
Polímeros como poli(p-dioxanona) – PPD, o poli (ácido lático) – PLA,poli (ácido glicólico) – PGA eseus copolíme-rosPLLAePLGAepoli(␣-hidroxiácidos)comcaracterísticas dedegradac¸ão,biorreabsorc¸ãoebiocompatibilidadetêmsido exaustivamenteestudados.4,21–24
Nonossoestudoempregamosumhidrogel nãoporosoe nãoabsorvível(PLDLA-co-TMC/PVA)parapreenchimentodo defeitoosteocondral,enãoparareparac¸ãoquepermita cres-cimentodeneotecido.
Arespostabiológicainvivocompinosdehidrogel PLDLA--co-TMC/PVAnopreenchimentodedefeitososteocondraisé desconhecida.
Oobjetivodeste trabalho foi avaliarodesempenho bio-lógicode arcabouc¸osde hidrogelPLDLA-co-TMC/PVA como implantenopreenchimento,enãonoreparo,dedefeito oste-ocondralemcoelhosNovaZelândiaeverificarainfluênciado materialnaprotec¸ãotecidualinvivo.
Material
e
métodos
Opresenteestudofoiaprovado pelaComissãodeÉtica em Pesquisa de nossa instituic¸ão (CEUA/FCMS/PUCSP, número 2013/10).
Preparac¸ãodosarcabouc¸ospoliméricos(pinosdehidrogel)
Os pinos de hidrogel são compostos por polímeros semi--interpenetrantesbaseadosemPoli(ÁlcoolVinílico)(PVA)e poli(L-co-D,L ácido lático)-co-trimetileno carbonato (PLDLA--TMC).Ohidrogelfoifeitocomumasoluc¸ãode10%m/vde PVAemáguae10%docompostoPLDLA-TMCemrelac¸ão à massadePVAusada.Asoluc¸ãofoientãovertidaemmoldesde PTFE(politetrafluoretileno)comdiâmetrode4,1mm,deixados emprocessodecongelamento-descongelamentodurantedois dias.Apósesseprocessoospinosforamretiradosdomolde, cortadosnosentidodocomprimentocom13mm, esteriliza-dosemradiac¸ãoUVeimplantados(fig.1).
Estudoinvivocomimplantedospinosecontroles
Foramusados12coelhosNovaZelândia,deambosossexos, entre120e150diase3,5kga4,5kg.
Apósjejumpré-operatóriodeoitohoras,submetemosos animaisàanestesiageralviaintramuscularcomcloridratode
Figura1–PinosdehidrogelPLDLA-co-TMC/PVAemolde usadoparaconfecc¸ãodosdispositivos.
cetamina(30mg/kgdepeso)associadoacloridratodexilazina (5mg/kgdepeso).Feitatricotomiada áreaoperada,os coe-lhosforamposicionadosemmesa cirúrgicaapropriada,em decúbitodorsalhorizontal.Aassepsiafoifeitacomsoluc¸ãode clorexidinaalcoólica0,5%aplicadacomgazesestéreis.O cirur-giãofezusodeluvascirúrgicasestéreisemateriaiscirúrgicos esterilizadosemautoclavea180◦Cporduashoras.
Usamos incisão para patelar medialcom dissecc¸ão por planos (subcutâneo e capsulotomia para patelar medial). Procedeu-seàluxac¸ãolateraldapatelaqueexpôsos côndi-losfemorais.Comojoelhofletidoa90◦,criou-seumdefeito cilíndriconacartilagemarticularenoossosubcondralno côn-dilofemoralmedialcomoempregoumabrocatrefinametálica de3,3mm/38,5mmefoiretiradoumcilindroosteocondralde 1cmdeprofundidadedeambososjoelhos7,13(figs.2e3).
Figura3–Implanteecilindroosteocondral.
Odefeitocondralfoicriadoemambososcôndilosfemorais mediais,emumdosladosfoiimplantadoopinodehidrogel (ladoimplante),enquantonooutro(ladocontrole)foiapenas mantidoodefeito(fig.4).
Foifeitasuturaporplanosapósalavagemcomsoro fisi-ológico0,9%enãoforamusadoscurativosouimobilizac¸ões. Todososanimaisforammantidosindividualmenteemgaiolas metálicas,comáguaerac¸ãoadlibitum.
Retiradadomaterial–Eutanásiaecoletadetecido
Apósnovesemanasforamsacrificadosseteanimaisecinco após16semanas.
Usamos inalac¸ão com halotano. Após a constatac¸ão da morte,oanimalfoiposicionadoemdecúbitodorsal horizon-tal. Dessa maneira foram ressecados os côndilos femorais mediais dos dois joelhos, por via de acesso para patelar medial.
Avaliac¸ãomacroscópica
Os côndilos foram individualmente identificados, observa-dos macroscopicamente e fotografados (fig. 5). De acordo comaclassificac¸ãodeOuterbridgemodificada,ogrupopino, tantocom novecomo16semanas–considerou-sequenão houvecrescimentode tecidosobreopino–gruponãopôde serincluídonaclassificac¸ão.Jánogrupocontrole,comnove ou16semanas,observaram-sealterac¸õescaracterísticasde OuterbridgeII.
Processamentodomaterial–Análisehistológica
Oscôndilosfemoraisforamcolocadosemrecipientesdevidro comsoluc¸ãodeBouin(compostadeácidopícrico,ácido acé-ticoeformaldeído)parafixac¸ãopor24horasquemantéma integridadedostecidosapósamorte.
O material foi descalcificados em EDTA 4,13% (soluc¸ão descalcificadoracompostadeEDTAtetrassódico,tartaratode sódio,tartaratodesódio epotássio,ácidoclorídricoeágua destilada)por21dias.
Para processamento histológico foram feitos cortes paralelos longitudinais (craniocaudais) e identificados sequencialmente para cada amostra. Essa técnica permi-tiu avaliac¸ão precisa de toda área do côndilo, incluindo a inicialmente lesada e toda a superfície ao redor da lesão.
Asamostras,devidamenteidentificadas,foram desidrata-das emumasequênciadesoluc¸õesalcoólicas,diafanizadas sequencialmenteemxilolI,IIeIIIeincluídasemparafinaa 70◦C.Apósocortede3m,asamostrasforamcoradascom Hematoxilina-Eosinaeanalisadaspormicroscopiadeluz con-vencional.
Figura5–A,compinodehidrogel;B,sempino(grupocontrole).
Avaliac¸ãomicroscópica
Noexamehistológicoqualitativodassecc¸õesdofêmur dis-tal,aatenc¸ãofoidirigida,particularmente,paraosseguintes elementos:
1. tipodetecidoquerecobriaasuperfíciearticular:cartilagem hialina,fibrocartilagem,tecidoósseooutecidofibroso; 2. estadodasuperfíciecartilaginosa:lisa,comdepressãoou
irregularcompresenc¸adefissurasoufragmentos; 3. padrãodoossosubcondral;
4. presenc¸aounãodenecroseerespostainflamatória propri-amentedita;
5. encontroounãodealterac¸õeshiperplásicasdacartilagem outecidoósseo;
6. avaliac¸ãodasmembranassinoviais,quandopossível.
Resultados
Naavaliac¸ãoderesultadosforamconsideradosquantidadede fibrose,neoformac¸ãoósseaepresenc¸adetecidocartilaginoso nasuperfíciecondilar.
Nogrupopino,sacrificadonovesemanasapósoimplante, encontramosfibrosediscretaemquatroanimais,fibrose acen-tuadaemdoisenenhumcomfibrosemoderada.
Nogrupocontrole,sacrificadonovesemanasapósacriac¸ão dodefeitoosteocondral,encontramosfibrosediscretaemdois animais,moderadaemdoiseacentuadaemdois.
Nogrupopino,sacrificadoapósnovesemanasdoimplante, umanimalapresentouneoformac¸ãoósseaeemcincoelanão foi encontrada. Jáno grupo controle, aneoformac¸ão óssea estavapresenteemquatroanimais,contraausênciaemum animal.
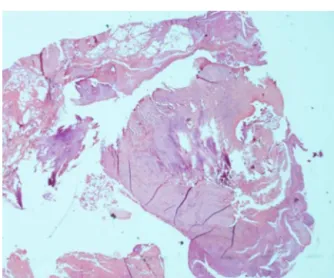
Comrelac¸ãoàpresenc¸adecartilagemnasuperfície articu-lar,nãofoiencontradaemquatrocoelhosdogrupocontrole eestavapresenteemumcaso.Emumdoscoelhosfoi encon-tradaumasuperfíciequenãopôdeserdefinidacomotecido cartilaginosoorganizado.Nogrupopinoocorreupresenc¸ade tecidocartilaginosoemquatrocasos,enquantoemdois coe-lhosnãofoiencontradacartilagem(tabela1efigs.6e7).
Um dos animais incluído no grupo sacrificado com 16 semanas apresentou infecc¸ão no sítio cirúrgico e foi excluídodotrabalho.
Quatrocoelhosdogrupopinoapresentaramfibrosedegrau discretoeumnãotevefibrose.
Aneoformac¸ãoósseaocorreuemquatrocoelhosdogrupo controleeemumdelesocorreufragmentac¸ãodomaterial,o queinviabilizou aanálisecorreta.Jánogrupopino nãofoi observadapresenc¸adeneoformac¸ãoóssea.
Nogrupocontrole,com16semanasocorreudegenerac¸ão de cartilagem em um caso, enquanto naquele com
Tabela1–Coelhosdogrupocomnovesemanas
Sacrifícionovesemanas Grupos Fibrose Neoformac¸ãoóssea Superfíciecartilaginosa
Coelho1-9 Controle Acentuada Ausente Ausente
Coelho1-9 Pino Discreta Ausente Presente
Coelho2-9 Controle Moderada Presente Desorganizada
Coelho2-9 Pino Acentuada Presente Ausente
Coelho3-9 Controle Discreta Presente Ausente
Coelho3-9 Pino Discreta Ausente Ausente
Coelho4-9 Controle Discreta Presente Ausente
Coelho4-9 Pino Discreta Ausente Presente
Coelho5-9 Controle Acentuada Presente Presente
Coelho5-9 Pino Discreta Ausente Presente
Coelho6-9 Controle Moderada Ausente Ausente
Figura6–Lâminahistológicadogrupopinonovesemanas comausênciadereac¸ãoinflamatóriaelevefibrose.
Figura7–Lâminahistológicadogrupocontrolecomnove semanascomneoformac¸ãoóssea,fibroseexuberante edesorganizac¸ãotecidual.
fragmentac¸ão do material não foi possível analisar a presenc¸aou não de cartilagem.Em dois coelhos dogrupo controle encontramos cartilagem na superfície articular contra um que não a apresentava. No grupo pino, cinco
Figura8–Lâminahistológicadogrupopinode16semanas quemostradiscretafibrose,semneoformac¸ãoóssea.
coelhos tinham cartilagem presente, contra um ausente (tabela2efigs.8e9).
Discussão
Dos 12coelhosestudados, apenasumdogruposacrificado comnovesemanasfoiexcluídoporapresentarinfecc¸ãolocal. Portanto,11animaisfizerampartedesteestudo.
A análise histológica dos implantes de arcabouc¸os de PLDLA-co-TMC/PVA após nove semanas evidenciou que o pino não induz reac¸ão inflamatória, tampouco estimula a neoformac¸ãoóssea.Háestimuloparaproliferac¸ãofibrosanas bordasdalesãoapartirdacartilagemarticularcomformac¸ão principalmentedefibrocartilagemetentativadefechamento dalesão.
Nogrupocontroleapósnovesemanashámaisfibrose,mais neoformac¸ãoóssea,sejaapartirdacartilagemarticulardas bordasdalesãocomoapartirdastrabéculasdoossocompacto
Tabela2–Coelhosdogrupocom16semanas
Sacrifício16semanas Grupos Fibrose Neoformac¸ãoóssea Superficiecartilaginosa
Coelho1-16 Controle Discreta Presente Presente
Coelho1-16 Pino Discreta Ausente Ausente
Coelho2-16 Controle Discreta Presente Presente
Coelho2-16 Pino Discreta Ausente Presente
Coelho3-16 Controle Discreta Presente Denerac¸ão
Coelho3-16 Pino Discreta Ausente Presente
Coelho4-16 Controle Fragmentac¸ão Análiseinviável
Coelho4-16 Pino Discreta Ausente Presente
Coelho5-16 Controle Moderada Presente Ausente
Figura9–Lâminahistológicadogrupocontrolede 16semanasquemostraneoformac¸ãoósseaefibrose.
rodeadasdecélulasosteoprogenitoras.Porém,semevidências dereparodalesãocondral.
Após16semanasoscôndiloscomimplantesdehidrogel nãoevidenciaramreac¸ãoinflamatóriaeestavamrodeadospor cápsulafibrosa.Oossotrabecularaoseuredortemaspecto conservado e há fechamento da superfície articular com presenc¸adecartilagemhialinaouentãocartilagematrófica deaspectofibro-hialino.
Naslesõesdogrupocontrolecom16semanashouvemais proliferac¸ãoósseanasáreasdodefeito.Noentanto,com car-tilagemarticulardesorganizada,comfibroseevidente,houve atrofiacomexposic¸ãoósseaeproliferac¸ãodemembrana sino-vial.
Comrelac¸ãoàneoformac¸ãoóssea,nogrupodenove sema-nas, para nossa surpresa, um dos animais do grupo pino apresentoucrescimentodetecidoósseocompadrãofibroso. Jáosoutroscoelhosdesse gruponão apresentaram cresci-mentoósseo,enquantoemtodosdogrupocontroleocorreu neoformac¸ãoóssea.
Nogrupocontrolesacrificadocom16semanas encontrou--se,como esperado, preenchimento ósseono defeito oste-ocondral, muito provavelmente devido ao maior tempo decorridoentreacirurgiaeosacrifício.Entretanto,nos ani-maisdogrupopinonãohouvecrescimentoósseonodefeito. Issosugerequeapresenc¸adopinoimplantadocausou preen-chimentodetodooespac¸ocriadopelodefeito.
Conclusão
Os pinos de hidrogel demonstraram superioridade com relac¸ãoàprotec¸ãodasuperfíciecartilaginosaarticular,como artefatos depreenchimento dosdefeitososteocondrais. No entanto, não apresentaram qualquer efeito reparador. Por outrolado,nogrupocontrole,verificou-sedegradac¸ãoda car-tilagemtantonodefeitoquantonaperiferia.
Conflitos
de
interesse
Osautoresdeclaramnãohaverconflitosdeinteresse.
r
e
f
e
r
ê
n
c
i
a
s
1.RedmanSN,OldfieldSF,ArcherCW.Currentstrategiesfor articularcartilagerepair.EurCellMater.2005;9:23–32. 2.SwieszkowskiW,TuanBH,KurzydlowskiKJ,HutmacherDW.
Repairandregenerationofosteochondraldefectsinthe articularjoints.BiomolEng.2007;24(5):489–95.
3.BuckwalterJA,EinhornTA,SimonSR,editors.Orthopaedic basicscience.Biologyandbiomechanicsofthe
musculoskeletalsystem.2nded.Rosemont,IL:AAOS;2000. 4.GarridoLF.Avaliac¸ãododesempenhodeimplantesde
polietilenoedefosfatotricalcio,recobertosporhidrogel, emdefeitososteocondraisnojoelhodecães.Campinas: UniversidadeEstadualdeCampinas,FaculdadedeCiências Médicas;2007.Dissertac¸ão.
5.LittleK.Natureofosteopetrosis.BrMedJ.1969;2(5648):49–50. 6.DingM,DalstraM,LindeF,HvidI.Mechanicalpropertiesof
thenormalhumantibialcartilage-bonecomplexinrelation toage.ClinBiomech(BristolAvon).1998;13(4-5):351–8. 7.SouzaTD,DelCarloRJ,ViloriaMIV.Efeitosdaeletroterapiano
processodareparac¸ãodasuperfíciearticulardecoelhos. CiêncRural.2001;31:819–24.
8.LammiPE,LammiMJ,TammiRH,HelminenHJ,EspanhaMM. Stronghyaluronanexpressioninthefull-thicknessrat articularcartilagerepairtissue.HistochemCellBiol. 2001;115(4):301–8.
9.SlatterD.Manualdecirurgiadepequenosanimais.Baureri, SP:Manole;1998.
10.RezendeUM,HernandezAJ,CamanhoGL,AmatuzziMM. Cartilagemarticulareosteoartrose.ActaOrtopBras. 2000;8(2):100–4.
11.MankinHJ.Theresponseofarticularcartilagetomechanical injury.JBoneJointSurgAm.1982;64(3):460–6.
12.CookSD,PatronLP,SalkeldSL,RuegerDC.Repairofarticular cartilagedefectswithosteogenicprotein-1(BMP-7)indogs. JBoneJointSurgAm.2003;85Suppl3:116–23.
13.RibeiroJL,CamanhoGL,TakitaLC.Estudomacroscópico ehistológicodereparososteocondraisbiologicamente aceitáveis.ActaOrtopBras.2004;12(1):16–21.
14.EspósitoAR,BonadioAC,PereiraNO,CardosoTP,BarboMLP, DuekEAR.TheuseofPLDLA/PCL-Tscaffoldtorepair osteochondraldefectsinvivo.MatRes.2013;16(1):105–15. 15.HuntleyJS,McBirnieJM,SimpsonAH,HallAC.Cutting-edge
designtoimprovecellviabilityinosteochondralgrafts. OsteoarthritisCartilage.2005;13(8):665–71.
16.HendersonI,FranciscoR,OakesB,CameronJ.Autologous chondrocyteimplantationfortreatmentoffocalchondral defectsoftheknee–Aclinical,arthroscopic,MRInand histologicevaluationat2years.Knee.2005;12(3): 209–16.
17.HattoriK,TakakuraY,OhgushiH,HabataT,UematsuK, IkeuchiK.Novelultrasonicevaluationoftissue-engineered cartilageforlargeosteochondraldefects–Non-invasive judgmentoftissue-engineeredcartilage.JOrthopRes. 2005;23(5):1179–83.
18.BumaP,RamrattanNN,vanTienenTG,VethRP.Tissue engineeringofthemeniscus.Biomaterials.
2004;25(9):1523–32.
19.MartinI,MiotS,BarberoA,JakobM,WendtD.Osteochondral tissueengineering.JBiomech.2007;40(4):750–65.
20.JansenEJ,PieperJ,GijbelsMJ,GuldemondNA,RiesleJ, VanRhijnLW,etal.PEOT/PBTbasedscaffoldswithlow mechanicalpropertiesimprovecartilagerepairtissue formationinosteochondraldefects.JBiomedMaterResA. 2009;89(2):444–52.
22.RahmanMS,TsuchiyaT.Enhancementofchondrogenic differentiationofhumanarticularchondrocytesby biodegradablepolymers.TissueEng.2001;7(6):781–90. 23.ZhaoK,DengY,ChunChenJ,ChenGQ.Polyhydroxyalkanoate
(PHA)scaffoldswithgoodmechanicalpropertiesand biocompatibility.Biomaterials.2003;24(6):1041–5.
24.SakataMM,Alberto-RinconMC,DuekEA.Estudodainterac¸ão polímero/cartilagem/ossoutilizandopoli(ácido
lático-co-ácidoglicólico)epoli(p-dionaxona)